【指南共识】冠心病合并心房颤动患者抗栓管理中国专家共识
发布时间:2020-10-28 11:46:20
本文刊于:
中华心血管病杂志, 2020,48(07): 552-564
单位:
中华医学会心血管病学分会
中华心血管病杂志编辑委员会
通信作者:
袁祖贻,Email:zuyiyuan@mail.xjtu.edu.cn
吴书林,Email:doctorwushulin@163.com
韩雅玲,Email:hanyaling@263.net
摘要
冠心病与心房颤动(房颤)合并存在临床并不少见。冠心病患者需要进行抗血小板治疗以减少心肌缺血事件,而血栓栓塞高风险的房颤患者则需口服抗凝药物以减少卒中等血栓栓塞事件。冠心病与房颤合并存在时,联合应用抗血小板与抗凝治疗可有效减少缺血及血栓栓塞事件,但会增加出血风险。针对冠心病合并房颤患者,如何选择最佳的抗栓方案一直是临床研究的热点。近年来,欧美等国家和地区相继发布了急性冠状动脉综合征和/或经皮冠状动脉介入治疗合并房颤患者的抗栓治疗专家共识并及时更新,而我国尚缺乏相应的抗栓治疗指南或共识。该共识依据已发表的临床研究证据,结合国内外相关指南、共识以及专家建议等,着眼于解决不同类型冠心病合并房颤患者抗栓治疗临床实践中的问题,对指导我国冠心病合并房颤患者的治疗意义重大。
冠心病与心房颤动(房颤)具有多种相同的危险因素,两种疾病常合并存在。冠心病患者合并房颤的比例为6%~21%[1],房颤患者合并冠心病的比例为20%~30%[2, 3, 4]。冠心病患者需要进行抗血小板治疗以减少心肌缺血事件,而血栓栓塞高风险的房颤患者则需口服抗凝药物(oral anticoagulant,OAC)治疗以减少卒中等血栓栓塞事件[5]。冠心病与房颤合并存在时,联合应用抗血小板与抗凝治疗可有效减少缺血及血栓栓塞事件,但增加出血风险[6]。冠心病合并房颤患者如何选择最佳的抗栓方案一直是临床研究的热点问题。近年来,欧洲[7, 8, 9]及北美[6, 10, 11]相继发布了急性冠状动脉综合征(acute coronary syndromes,ACS)和/或经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)合并房颤患者抗栓治疗的专家共识,并均已陆续更新至第3版。我国虽已发表了一系列冠心病或房颤相关指南或共识,但尚缺乏针对冠心病合并房颤患者抗栓治疗的指南或共识。
本共识依据已发表的临床研究证据,结合国内外相关指南或共识以及专家建议,着眼于解决不同类型冠心病合并房颤患者抗栓治疗临床实践中的问题。本共识对相关文献进行了系统性回顾,并评估了证据强度。对于缺乏证据的领域,根据本共识撰写专家组的讨论结果做出相应的推荐。为了让临床医生能更简单地理解当前的证据强度及相应的推荐状态,本共识采用“++”、“+/±”及“-”表示不同的推荐分类(表1)。
缺血和出血风险评估
为了提高抗栓治疗的获益并减少出血风险,在启动抗栓治疗前应对患者的血栓栓塞/缺血风险和出血风险进行评估。
一、血栓栓塞/卒中风险
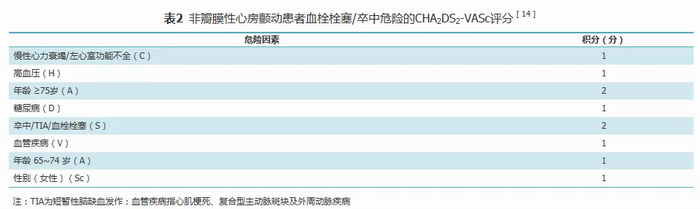
血栓栓塞事件是房颤致死、致残的主要原因,而卒中则是房颤栓塞最常见的表现类型[12]。房颤患者的血栓栓塞风险是连续且不断变化的,应定期进行评估[13]。目前推荐对所有非瓣膜性房颤(NVAF)患者采用CHA2DS2-VASc评分(表2)进行血栓栓塞风险评估[14]。近期发表的4项冠心病合并房颤的随机对照试验(RCT)均采用了CHA2DS2-VASc评分[15, 16, 17, 18]。
关于冠心病合并NVAF患者抗凝治疗的推荐[12, 13, 19, 20]:(1)CHA2DS2-VASc评分≥2分(男性)/3分(女性)的患者应进行长期抗凝治疗;(2)对于依从性较好、CHA2DS2-VASc评分为1分(男)/2分(女)的患者也建议进行抗凝治疗;(3)CHA2DS2-VASc评分为0分(男)/1分(女)的患者应避免抗凝治疗,预防血栓栓塞。目前认为,阵发性房颤与持续性或永久性房颤危险性相同,抗凝治疗的方法均取决于患者的危险分层;心房扑动的抗凝原则与房颤相同[21]。瓣膜性房颤具有明确抗凝适应证,无需再进行血栓栓塞风险评估。
二、缺血/血栓形成风险(表3)
心脏缺血事件最强的预测因素是近1年内发生过缺血事件[22]。既往有ACS病史的患者缺血事件风险远远高于稳定性冠心病患者,且对于支架置入的患者同样适用[23]。高龄、糖尿病、慢性肾脏病(肌酐清除率15~59 ml/min)、弥漫性冠状动脉病变、左心室射血分数低、支架选择不合理等均是缺血事件的重要危险因素[6]。
可采用SYNTAX[24]、SYNTAXⅡ[25](表4)或GRACE评分[26] 对PCI合并房颤患者进行缺血事件风险评估。SYNTAX和GRACE评分对于冠状动脉支架置入合并房颤患者的冠状动脉事件和死亡风险均有预测价值[27]。可根据SYNTAX和SYNTAXⅡ评分评估择期PCI患者中、远期缺血事件的风险[28, 29]。可采用GRACE评分对ACS患者进行院内及院外死亡风险评估[30]。GRACE评分对中国非ST段抬高型心肌梗死患者院内死亡率的预测价值优于TIMI评分[31]。
三、出血风险
出血风险与抗栓药物及抗栓治疗强度有关。对于采用单一抗血小板药物治疗的患者,阿司匹林与氯吡格雷总体出血风险相似,但是服用氯吡格雷患者因胃肠道出血的住院率较低[32]。普拉格雷和替格瑞洛出血风险高于氯吡格雷[33, 34]。非维生素K 拮抗剂口服抗凝药物(NOAC)大出血及致死性出血风险低于华法林[19]。既往出血史、高龄、低体重、慢性肾脏病(透析或肌酐清除率<15 ml/min)、糖尿病、贫血、长期使用类固醇或非甾体类抗炎药(NSAID)等均是出血的高危因素(表3)。
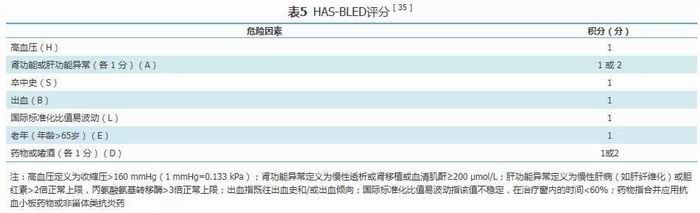
冠心病合并房颤患者出血风险评估推荐采用HAS-BLED评分(表5)[35]。出血风险评估主要是用于筛查可逆性出血危险因素,如高血压控制不理想(收缩压>160 mmHg,1 mmHg=0.133 kPa)、国际标准化比值(INR)不稳定、合用可能增加出血风险的药物(例如NSAID等)以及酗酒等[6]。HAS-BLED评分≥3分提示出血风险增加,但不应将出血风险增加视为抗栓治疗的禁忌证,应注意筛查并纠正可逆性的出血危险因素,并在开始抗栓治疗后加强随访和监测[13,19]。
抗栓治疗
一、ACS和/或PCI合并房颤患者的抗栓治疗
(一)循证医学证据(表6)
前已发表了多项评价不同抗栓治疗方案对于ACS和/或PCI合并房颤患者疗效和安全性的RCT[15, 16, 17, 18, 36, 37]。
WOEST[36]、PIONEER AF-PCI[15]、RE-DUAL PCI[16]及AUGUSTUS[17]研究均证实,与传统三联抗栓治疗相比,双联抗栓治疗明显降低了出血事件风险,且不增加缺血事件风险。但ENTRUST-AF PCI研究结果显示,以艾多沙班为基础的双联抗栓治疗与三联抗栓治疗患者发生出血和缺血事件的风险均相似[18]。ISAR-TRIPLE研究结果显示,三联抗栓治疗6周与6个月患者缺血和出血复合终点、缺血终点和出血终点差异均无统计学意义[37]。近期发表的一项荟萃分析纳入了WOEST、PIONEER AF-PCI、RE-DUAL PCI和AUGUSTUS 4项研究,结果显示双联抗栓治疗较三联抗栓治疗降低出血风险的效果更为显著,而对主要不良心血管事件发生率的影响相似[38]。另外一项荟萃分析纳入了4项关于NOAC的研究,结果显示NOAC+P2Y12受体拮抗剂较三联抗栓治疗降低出血风险(尤其大出血和颅内出血)的效果更为显著,但增加了支架内血栓的风险,同时心肌梗死风险也呈增加趋势,全因死亡、心血管死亡及卒中风险则相当[39]。
目前已发表了大量关于采用OAC治疗ACS和/或PCI合并房颤患者的观察性队列研究[9]。总体上,三联抗栓治疗与其他抗栓方案相比,显著增加了出血风险。出血风险可能与抗凝质量(INR的稳定性)呈负相关[40]。出血危险因素对大出血风险的影响可能大于联合抗栓方案本身[41]。不同抗栓方案主要不良心脑血管事件发生率相似。对于CHA2DS2-VASc评分为1分的PCI合并房颤患者,与双联抗血小板治疗(dual antiplatelet therapy,DAPT)相比,三联抗栓治疗并不能减少卒中和/或体循环栓塞风险,且增加出血风险[42]。由于观察性队列研究存在众多局限性,结果解读应谨慎[9]。包含新型更强效P2Y12受体拮抗剂(普拉格雷和替格瑞洛)的三联抗栓治疗与出血事件风险增加相关。
(二)抗栓治疗方案
1.急性期抗栓治疗:
所有OAC治疗的房颤患者在发生ACS后应立即口服负荷剂量阿司匹林(100~300 mg),然后维持剂量为75~100 mg/d。在已了解冠状动脉解剖结构或紧急情况下,如很可能行PCI,可考虑采用P2Y12受体拮抗剂进行预处理(图1);在不了解冠状动脉解剖结构时,应延迟至行PCI时再使用P2Y12受体拮抗剂进行预处理[9]。与氯吡格雷相比,普拉格雷和替格瑞洛虽然效果更为明显,但出血风险也更高[33, 34],因此P2Y12受体拮抗剂应首选氯吡格雷[9,11]。对于使用VKA的患者,氯吡格雷负荷剂量一般选择300 mg [9];由于数据有限,无论是否中断NOAC治疗,氯吡格雷负荷剂量根据常规临床实践建议选择300或600 mg[9]。对于缺血/血栓(如ACS)风险高、出血风险低的患者,替格瑞洛可能是合理的选择;替格瑞洛负荷剂量为180 mg,维持剂量为90 mg每日2次;若P2Y12受体拮抗剂选择替格瑞洛,则不建议使用阿司匹林(避免三联治疗)[11]。普拉格雷联合NOAC治疗的数据非常有限,一项小样本研究显示含普拉格雷的三联治疗出血风险增加4倍[43]。
PCI:经皮冠状动脉介入治疗,DES:药物洗脱支架,OAC:口服抗凝药物,DAPT:双联抗血小板治疗,SAPT:单一抗血小板治疗,PPI:质子泵抑制剂,NSAID:非甾体类抗炎药,NOAC:非维生素K拮抗剂口服抗凝药物,VKA:维生素K拮抗剂
图1 需OAC治疗的心房颤动患者PCI围术期抗栓管理流程
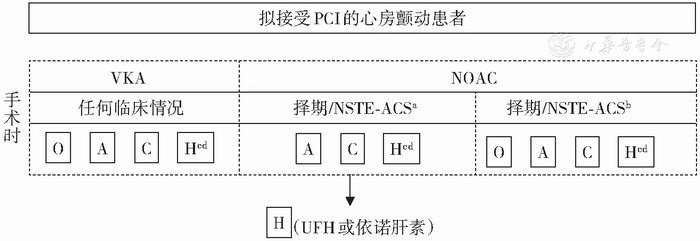
对于VKA治疗且行冠状动脉造影和/或PCI的患者,中断VKA并不能减少出血,中断VKA同时用肝素桥接可能增加出血,因此术前通常无需停用VKA,但需查INR。术中应使用普通肝素预防桡动脉闭塞,并可能减少术中血栓栓塞事件,但应监测活化凝血时间(ACT)。由于正在使用VKA治疗,普通肝素应采用低剂量(30~50 U/kg),并在ACT(维持≥225 s)指导下使用(图2)[9,29]。
PCI:经皮冠状动脉介入治疗,VKA:维生素K拮抗剂,NOAC:非维生素K 拮抗剂口服抗凝药物,NSTE-ACS:非ST段抬高型急性冠状动脉综合征, O:口服抗凝药物, A:阿司匹林,C:氯吡格雷,H:肝素,UFH:普通肝素;aNOAC及时中断,bNOAC没有及时中断,c减少剂量,d可考虑比伐芦定作为替代
图2 心房颤动患者PCI术中抗栓策略
对于NOAC治疗的患者,急诊PCI无需中断NOAC。而择期PCI则可考虑在术前停药,停药时间取决于使用的药物和肾功能(通常术前停药12~24 h,达比加群酯经肾脏清除率较高,肾功能不全者需考虑延长术前停药时间),均无需桥接治疗。无论NOAC是否中断治疗,术中均需在ACT指导下使用肝素治疗。PCI术后早期,如当天晚上或次日早晨,建议开始NOAC(术前剂量)治疗[9]。
术中抗凝除了肝素类药物,也可考虑采用比伐芦定(一次性静脉注射0.75 mg/kg,随后1.75 mg·kg-1·h-1,维持至术后3~4 h)作为替代,但不推荐使用磺达肝癸钠[9,29]。BRIGHT研究采用延时注射高剂量比伐芦定(PCI术后持续静脉滴注术中剂量的比伐芦定3~4 h),发现与肝素或肝素联合血小板膜糖蛋白Ⅱb/Ⅲa 受体拮抗剂(glycoprotein Ⅱb/Ⅲa receptor inhibitor,GPI)相比,应用比伐芦定可减少净不良事件和出血风险,且不增加支架内血栓风险[44]。荟萃分析表明,与肝素或低分子肝素联合GPI相比比伐芦定出血风险最低[45]。
2.术后及出院后抗栓治疗:
本共识推荐大多数患者出院后采用OAC+P2Y12受体拮抗剂的双联抗栓治疗(图1)[11]。无论支架类型如何,双联抗栓治疗的获益都是一致的[15, 16, 17, 18]。
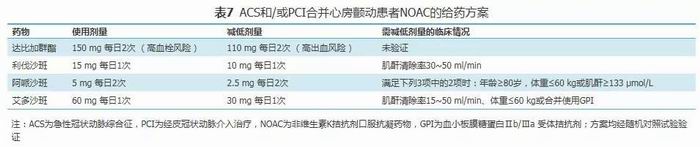
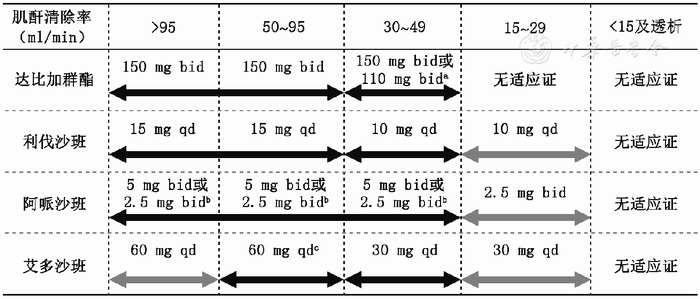
OAC治疗:如无禁忌证,大多数冠状动脉支架术后合并房颤患者应首选NOAC,而非VKA[9,11]。由于缺乏不同NOAC头对头比较的研究,暂无优先使用何种NOAC的建议[11]。NOAC应根据RCT(PIONEER AF-PCI、RE-DUAL PCI、AUGUSTUS和ENTRUST-AF PCI研究等)验证的给药方式给药(表7)[15, 16, 17, 18]。RE-DUAL PCI研究结果显示,与三联治疗相比,达比加群酯110 mg每日2次为基础的双联抗栓治疗有增加缺血事件风险的趋势(但差异无统计学意义,HR=1.51,95%CI 0.94~2.41,P=0.09)[16],因此血栓栓塞风险较高者推荐150 mg每日2次,而出血风险较高者可选择110 mg每日2次。利伐沙班预防房颤卒中的标准剂量是20 mg每日1次,PIONEER AF-PCI研究针对ACS和/或PCI合并房颤患者,采用利伐沙班15 mg每日1次+P2Y12受体拮抗剂及利伐沙班2.5 mg每日2次+DAPT两种方案[15],推荐采用利伐沙班15 mg每日1次的双联抗栓方案预防卒中[9,11]。对于PCI术前使用VKA的患者,在患者INR控制良好且无血栓栓塞/出血并发症的前提下术后可继续使用VKA;合并中重度二尖瓣狭窄或机械人工心脏瓣膜患者选择VKA;合并严重肾功能不全患者(透析或肌酐清除率<15 ml/min),现阶段仍首选VKA,INR目标值为治疗范围下限(2.0~2.5)[9,11]。具有抗凝指征的房颤患者如无禁忌证,应终生持续抗凝治疗。
抗血小板治疗:对于考虑采用双联抗栓治疗的患者,PCI围术期需加用阿司匹林(三联治疗)直至出院。对于高缺血/血栓栓塞和低出血风险的患者,出院后阿司匹林可继续使用至术后1个月,但很少超过1个月[11]。大多数双联抗栓的患者应考虑在术后1年时停用抗血小板治疗;低缺血/血栓栓塞和高出血风险的患者可在PCI 术后6个月停用抗血小板治疗;高缺血/血栓栓塞和低出血风险的患者,1年后继续双联抗栓治疗可能是合理的(图1)。PCI术后1年由医师决定选用何种抗血小板药物(阿司匹林或氯吡格雷),建议继续服用之前的抗血小板药物、不换药[11]。
停用抗血小板治疗药物后,应继续给予卒中预防剂量的OAC。双联抗栓治疗时如采用低剂量利伐沙班(15 mg每日1次,肌酐清除率30~50 ml/min时10 mg每日1次),在停用抗血小板治疗药物后应采用足剂量利伐沙班(20 mg每日1次,肌酐清除率30~50 ml/min时15 mg每日1次)[11]。
3.房颤患者PCI围术期注意事项:房颤患者PCI围术期应综合考虑多方面因素(图1),如术前应考虑PCI适应证和风险评估,术中考虑血管径路和支架选择,术后应定期进行风险评估,推荐使用质子泵抑制剂(PPI),避免使用NSAID等[6,11]。
术前注意事项[6,11]:(1)PCI适应证:需OAC治疗的PCI患者优化抗栓治疗较为复杂,因此应严格掌握PCI适应证。建议根据《中国经皮冠状动脉介入治疗指南(2016)》[29]选择适合PCI的患者。ACS患者以及强化药物治疗的情况下仍存在缺血症状、存在较大范围心肌缺血证据且预判PCI潜在获益大于风险的稳定性冠心病患者可考虑进行血运重建。对血运重建获益不明确的患者建议保守抗栓治疗。(2)风险评估:对于需OAC联合抗血小板治疗的患者,应根据其特征制定详细的治疗策略。风险评分可辅助筛查缺血、血栓栓塞及出血事件高风险患者,并有助于明确抗栓治疗的强度和疗程。对于同时存在缺血/血栓栓塞及出血事件高风险的患者,应详细权衡每种药物的获益与风险,同时考虑患者意愿。在确定抗栓治疗强度和疗程时,应动态评估患者的血栓栓塞和出血风险。
术中注意事项[6,11]:PCI患者采用桡动脉径路可减少出血风险[46]。对于高出血风险的患者,包括需联合抗血小板、抗凝治疗的患者,应首选桡动脉径路。OAC治疗患者如术前不能中断抗凝或PCI时INR处于治疗范围,桡动脉径路可能更安全。基于安全性和疗效,推荐首选新一代药物洗脱支架[6]。目前生物可降解支架仍缺乏循证医学证据。
术后注意事项[6,11]:PCI及起始OAC治疗后早期缺血和出血风险较高,术后前几个月应密切监测。VKA治疗患者INR波动性大,更应密切监测(尤其在治疗早期)。NOAC治疗患者应监测肾功能,必要时调整剂量[47]。不应因小出血或瘀斑而随意停止抗栓治疗,而应及时就诊。应定期评估患者缺血和出血风险,以及时调整治疗方案。
术后推荐使用PPI、避免使用NSAID:可考虑使用PPI以减少胃肠道出血,尤其对于联合抗栓治疗的患者。PPI与氯吡格雷之间的相互作用并非类效应,仅与抑制P450 2C19活性的PPI(如奥美拉唑和埃索美拉唑)有相互作用。因此,应首选不影响P450 2C19活性的PPI(如泮托拉唑和雷贝拉唑等)。应避免使用NSAID,因其可影响阿司匹林疗效,同时增加出血风险和血栓风险。
二、稳定性冠心病合并房颤患者的抗栓治疗
(一)循证医学证据
AFIRE研究是日本的一项针对稳定性冠心病合并房颤患者的RCT [48],其结果显示利伐沙班单药治疗组(肌酐清除率≥50 ml/min者15 mg/d,15~49 ml/min者10 mg/d)患者心血管事件或全因死亡复合终点不劣于联合治疗组(利伐沙班+1种抗血小板药物),而大出血发生率则低于联合治疗组。
(二)稳定性冠心病合并房颤的抗栓治疗
根据CHA2DS2-VASc评分,如稳定性冠心病合并房颤患者具有抗凝指征,推荐应用卒中预防剂量的OAC单药治疗[9]。对于具有高缺血风险、无高出血风险的患者可考虑在长期OAC(如利伐沙班)基础上加用阿司匹林75~100 mg/d(或氯吡格雷75 mg/d)[49]。对于适合NOAC的患者,推荐NOAC优于VKA[9,11]。
高缺血风险,即弥漫性多支病变的冠心病,且伴以下至少1种情况:(1)需药物治疗的糖尿病;(2)再发心肌梗死;(3)外周动脉疾病;(4)估算的肾小球滤过率(eGFR)15~59 ml·min-1·1.73 m-2。
高出血风险:(1)既往有脑出血或缺血性卒中史;(2)其他颅内疾病史;(3)近期胃肠道出血或胃肠道出血导致的贫血;(4)与出血风险增加相关的其他胃肠道疾病;(5)肝功能不全;(6)出血倾向或凝血障碍;(7)高龄或体弱;(8)需透析或eGFR<15 ml·min-1·1.73 m-2。
特殊情况的抗栓治疗
一、非心脏外科手术围术期
(一)抗凝治疗
1.应用华法林患者围术期的用药推荐[19]:
(1)术前准备:低出血风险手术且患者无出血危险因素(出血危险因素包括3个月内有大出血或颅内出血史,血小板质量或数量异常,有桥接出血史或接受类似手术出血史等),可不中断华法林治疗,但术前应严密监测INR,确定其位于治疗目标范围(2.0~3.0)。高出血风险手术和/或患者伴有出血危险因素,术前应中断华法林治疗。围术期中断华法林的时间主要取决于手术出血风险和当前的INR值,所有患者应在术前5~7 d测定INR。若手术要求INR值完全在正常范围, INR在1.5~1.9时术前需要停用华法林3~4 d,当INR≥2.0时术前停用华法林至少5 d。INR 持续升高者,应尽可能推迟手术日期,直至INR恢复正常。(2)术后管理:根据手术出血情况,在术后12~24 h重新开始抗凝治疗。出血风险高的手术,可延迟至术后48~72 h再重启抗凝,术后可采用普通肝素或低分子肝素与华法林桥接,INR达标后停用普通肝素或低分子肝素。
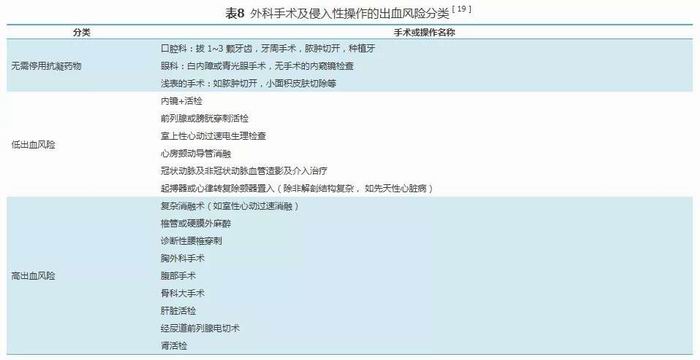
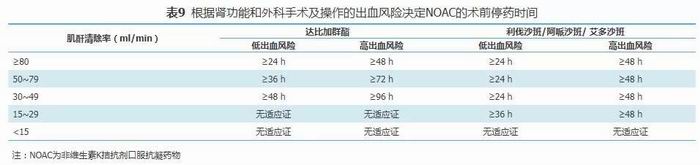
2.应用NOAC患者围术期的用药推荐[19]:
低出血风险及出血容易控制的手术无需中断NOAC治疗。NOAC停药时间依具体手术操作的出血风险(表8)、肌酐清除率和所使用的药物种类而定(表9)。低出血风险手术在术后数小时可重启抗凝治疗,高出血风险手术可在术后24~72 h重启抗凝治疗。
(二)抗血小板治疗[50]
服用阿司匹林进行二级预防的患者,在大多数非心脏外科手术围术期无需停药,密闭腔隙手术(如颅内神经外科手术、眼后房手术、椎管手术等)或出血风险很高时可于术前5 d停用。P2Y12 受体拮抗剂(氯吡格雷或替格瑞洛)可增加外科手术围术期出血风险,如缺血风险较低,应于术前5 d停用;如缺血风险较高,术前5 d停用 P2Y12 受体拮抗剂,并换为静脉GPI作为桥接治疗,直至术前4 h。术后应尽早恢复抗血小板治疗(最好在24 h内)。
二、冠状动脉旁路移植术(coronary artery bypass grafting,CABG)围术期
抗凝治疗:华法林和NOAC在围术期的用药可参考非心脏外科手术围术期的抗凝治疗[19]。
抗血小板治疗[51]:(1)阿司匹林围术期的用药推荐:拟行CABG的患者应在术前每日给予阿司匹林100 mg,原则上术前不必停用阿司匹林。病情稳定、无出血的患者,术后6 h应恢复阿司匹林治疗(可经胃管给药)。(2)P2Y12受体拮抗剂:氯吡格雷和替格瑞洛在术前需停服5 d以上,而普拉格雷需停服7 d以上;对于急诊或需尽快CABG的患者,氯吡格雷和替格瑞洛至少停服24 h,以减少严重出血并发症。术后应尽早恢复P2Y12受体拮抗剂治疗(最好在24 h内)。
三、房颤导管消融围术期
术前已服用华法林或NOAC的患者,围术期无需中断抗凝治疗[13,19]。研究显示在不中断NOAC的情况下行导管消融术是安全的[52, 53, 54, 55]。
目前房颤导管消融围术期抗血小板应用尚缺乏循证医学证据。鉴于房颤导管消融术本身出血风险低,结合围术期抗凝的研究证据,建议无需中断抗血小板治疗。已应用双联抗栓治疗的患者(OAC+1种抗血小板药物),如不是特别紧急,可延期至停用抗血小板药物后再行导管消融术。
四、高龄患者(≥75岁)
高龄冠心病合并房颤患者是血栓栓塞高危人群,其抗栓策略可根据缺血/血栓风险和出血风险确定(图1)[11]。高龄患者常存在多种合并症,如痴呆、易跌倒、慢性肾脏病、贫血、高血压、糖尿病和认知功能障碍等,其对患者生活质量的影响可能超过房颤相关症状[13]。肝肾功能不全及同时使用多种药物,可能增加药物间相互作用及不良反应风险。建议对高龄患者加强综合管理,并适当调整抗凝药物剂量[56]。
五、肾功能不全患者
肾功能不全患者血栓栓塞及出血风险均增加,接受NOAC治疗的患者可根据肾功能调整剂量。
ACS和/或PCI合并房颤患者:NOAC在不同肾功能时的给药剂量参见表7和图3。荟萃分析结果显示华法林并不能减少透析的房颤患者死亡、卒中或缺血事件,且增加大出血事件,但严重肾功能不全的患者(透析或肌酐清除率<15 ml/min)抗凝仍首选VKA[57]。基于近期的回顾性研究[58],2019年美国房颤指南认为阿哌沙班可考虑用于终末期肾病(肌酐清除率<15 ml/min)或透析的NVAF患者[20]。最近也有回顾性研究表明,对于合并慢性肾脏病4~5期或血液透析的NVAF患者,利伐沙班疗效与华法林相似,且其可显著降低大出血风险33%[59]。
ACS:急性冠状动脉综合征,PCI:经皮冠状动脉介入治疗,NOAC:非维生素K拮抗剂口服抗凝药物,bid:每日2次,qd:每日1次;a高出血风险患者110 mg每日2次;b满足下列3项中任意2项使用2.5 mg每日2次:年龄≥80岁,体重≤60 kg,肌酐≥133 μmol/L;c可能适用其他剂量减量标准(体重≤60 kg,合并血小板膜糖蛋白Ⅱb/Ⅲa 受体拮抗剂治疗);灰色箭头表示慎用(重度肾功能不全患者Xa因子抑制剂应减量并慎用;艾多沙班在肌酐清除率升高的情况下,疗效有降低的趋势,需谨慎评估患者血栓栓塞和出血风险后,才可用于高肌酐清除率的非瓣膜性心房颤动患者);黑色箭头表示可常规使用
图3 ACS和/或PCI合并心房颤动患者不同肾功能状态下NOAC使用剂量推荐
稳定性冠心病合并房颤患者:采用NOAC单药治疗时,可根据肾功能不全程度调整剂量[19]。利伐沙班在肌酐清除率≥50 ml/min时采用20 mg每日1次,肌酐清除率30~49 ml/min时采用15 mg每日1次,肌酐清除率15~29 ml/min时可慎用15 mg每日1次。其他NOAC使用剂量的推荐参考图3。
六、胃肠道疾病
七、瓣膜性房颤
瓣膜性房颤定义为人工机械瓣膜置换或中重度二尖瓣狭窄时发生的房颤。瓣膜性房颤患者的抗凝治疗应选用华法林。ACS和/或PCI合并瓣膜性房颤患者的抗血小板治疗策略,可参考“ACS和/或PCI合并房颤患者的抗栓治疗”一节。
八、华法林与NOAC之间的转换[47]
由华法林转为NOAC:如患者从华法林转换为NOAC,应先停用华法林,密切监测INR。INR≤2.0时可立即给予NOAC。2.0<inr≤2.5时可立即或最好第2天给予noac。inr>2.5时,应每1~3 d监测1次INR,到上述范围再开始给药。</inr≤2.5时可立即或最好第2天给予noac。
由NOAC转为华法林:如患者从NOAC转换为华法林,应继续服用NOAC(艾多沙班剂量减半,其他NOAC剂量不变),并重叠使用华法林。华法林从标准剂量起始,并根据INR调整剂量。如INR<2.0,应在1~3 d后重复检测INR(NOAC给药之前检测INR)。直至INR≥2.0时停用NOAC,并在1 d后重复检测INR。停用NOAC后第1个月内应严密监测INR,直至INR稳定(即至少连续3次INR为2.0~3.0)。
房颤抗栓治疗用药管理、监测及出血的处理
NOAC治疗的患者无需常规监测凝血功能。华法林治疗应定期监测INR,并据此调整剂量(INR目标值在联合抗栓时为2.0~2.5[9,11]、单药治疗时为2.0~3.0,治疗目标范围内时间>65%)。华法林起始治疗时应每周监测INR 1~2次,抗凝强度稳定后(连续3次监测INR均在治疗窗内),每月复查1~2次;如以往INR一直很稳定,偶尔出现INR 升高,若不超过3.5,可暂时不调整剂量,2 d后复查INR;如抗凝过度(INR>4.0)但不伴有出血,可停药1次或数次,一般在停用华法林3 d后INR会降至目标范围。
二、出血的处理
出血的评估内容应包括出血部位、发生时间、严重程度、最后一次服用抗凝药物的时间及其他影响出血的因素,如肝肾功能、嗜酒、合并用药、既往出血史等。一般将出血程度分为轻微(鼻衄、皮肤小瘀斑、轻微外伤后出血)、中度(肉眼血尿、自发大片瘀斑、无血流动力学障碍而需输血治疗)、严重(具有生命危险的出血,包括关键部位出血,如颅内出血和腹膜后出血及导致血流动力学不稳定的出血)[19,63]。
轻微出血:建议给予支持治疗,如机械压迫止血或小手术止血。口服华法林者可推迟给药时间或暂停给药,直至INR降至<2.0。NOAC的半衰期较短,停药12~24 h后凝血功能即可改善。
中度出血:可能需补液、输血治疗,需立即查找出血原因并给予相应治疗。服用华法林者可给予维生素K1(1~10 mg)静脉注射。NOAC最近一次服药时间在2~4 h内,口服活性炭和/或洗胃可减少药物吸收。达比加群酯可通过血液透析清除,但其他NOAC不适合透析清除。
严重出血:需即刻逆转抗凝药物的抗凝作用。服用华法林者首选输注凝血酶原复合物,其次可输注新鲜冰冻血浆,如病情需要可考虑输注血小板治疗,并可给予维生素K1(1~10 mg)静脉注射。应用NOAC者应给予特异性拮抗剂逆转其抗凝作用。依达赛珠单抗是逆转达比加群酯抗凝活性的单克隆抗体片段,输注后可快速逆转达比加群酯的抗凝作用,无促凝作用[64],已被美国食品药品监督管理局(FDA)、欧洲药品管理局和中国国家药品监督管理局批准使用。Andexanet α是一种改良重组人Xa,但不具有Xa活性,给药数分钟后就能逆转直接Xa因子抑制剂的抗凝作用,短暂增加凝血活性[65, 66],现已经美国FDA批准在出现危及生命或无法控制的出血时用于逆转Xa因子抑制剂的抗凝作用。
多数大出血有明确病因或诱因,应进行对因治疗。出血停止后常需重启抗凝治疗。临床决策困难时,可由多学科协同决定,权衡缺血/血栓栓塞和出血再发风险,并考虑患者意愿[19]。
三、患者教育
建议针对疾病、危险因素和治疗策略对患者进行教育,教育内容包括冠心病和房颤相关的疾病知识、不适症状的识别、发病后的自救及长期管理等,并教会患者监测血压和脉搏,使其充分了解自己的病情,缓解紧张情绪,提高治疗依从性和自信心。随访期间告知患者一旦发生出血,或冠心病/房颤一旦复发如何处理,并教育患者通过改变生活方式控制出血危险因素。
共识声明
ACS和/或PCI合并房颤患者应在保证抗栓效果的前提下尽可能缩短三联抗栓疗程,继以OAC加单一抗血小板药物(首选氯吡格雷75 mg每日1次)的双联抗栓治疗。三联抗栓疗程取决于缺血/血栓栓塞及出血风险。稳定性冠心病合并房颤患者如具有抗凝指征,推荐卒中预防剂量的OAC单药治疗。
冠心病合并房颤患者抗栓管理专家推荐意见总结如表10。
执笔专家:
曲鹏(大连医科大学附属第二医院),刘少稳(上海市第一人民医院),马长生(首都医科大学附属北京安贞医院),薛玉梅(广东省人民医院),雷新军(西安交通大学第一附属医院)
核心专家组成员(按姓氏拼音排序):
韩雅玲(北部战区总医院),黄岚(陆军军医大学新桥医院),李树岩(吉林大学第一医院),李毅(北部战区总医院),刘少稳(上海市第一人民医院),马长生(首都医科大学附属北京安贞医院),齐晓勇(河北省人民医院),曲鹏(大连医科大学附属第二医院),王祖禄(北部战区总医院),吴书林(广东省人民医院),袁祖贻(西安交通大学第一附属医院)
专家组成员(按姓氏拼音排序):
陈纪言(广东省人民医院),傅国胜(浙江大学医学院附属邵逸夫医院),高传玉(华中阜外心血管病医院),高炜(北京大学第三医院),贾绍斌(宁夏医科大学总医院),蒋晨阳(浙江大学医学院附属邵逸夫医院),雷新军(西安交通大学第一附属医院),李毅刚(上海交通大学医学院附属新华医院),刘启明(中南大学湘雅二医院),刘学波(同济大学附属同济医院),刘宇扬(首都医科大学附属北京安贞医院),娄大元(大连医科大学附属第二医院),鲁志兵(武汉大学中南医院),罗永百(西安交通大学第一附属医院),孙艺红(中日友好医院),唐熠达(中国医学科学院阜外医院),吴永健(中国医学科学院阜外医院),徐亚伟(上海市第十人民医院),薛玉梅(广东省人民医院),杨丽霞(解放军联勤保障部队第九二〇医院),杨新春(首都医科大学附属北京朝阳医院),杨艳敏(中国医学科学院阜外医院),殷跃辉(重庆医科大学附属第二医院),袁晋青(中国医学科学院阜外医院),张萍(北京清华长庚医院),张瑞岩(上海交通大学医学院附属瑞金医院),张抒扬(中国医学科学院北京协和医院),张钲(兰州大学第一医院)
参考文献 略
来源:中华心血管病杂志