【指南与共识】中国心血管病一级预防指南
发布时间:2020-12-25 15:39:03
本文刊于:中华心血管病杂志, 2020,48(12):1000-1038
作者:
中华医学会心血管病学分会
中国康复医学会心脏预防与康复专业委员会
中国老年学和老年医学会心脏专业委员会
中国医师协会心血管内科医师分会血栓防治专业委员会
通信作者:
胡大一,Email:dayiboai@163.com;
韩雅玲,Email:hanyaling@263.net;
宁光,Email:gning@sibs.ac.cn;
马长生,Email:chshma@vip.sina.com
摘要
心血管病是我国人群的首位死亡原因。实践证明,以生活方式干预和危险因素防控为核心的心血管病一级预防可有效延缓或避免心血管事件的发生。为全面推广健康生活方式并进一步规范高血压、血脂异常和糖尿病等心血管病危险因素的检出、诊断和治疗,提高心血管病一级预防的整体水平,由中华医学会心血管病学分会牵头组织国内多学科专家,遵循国内外指南撰写规范,汇总评价最新研究证据并参考相关指南,最终形成适合我国人群的心血管病一级预防的推荐意见。该指南包括前言、指南制定的方法学、心血管病流行病学现状、一级预防的总体建议、心血管病风险评估、生活方式干预、血脂管理、血压管理、2型糖尿病管理以及阿司匹林的使用10部分内容。该指南的颁布和实施将为推进我国心血管病预防实践发挥积极作用。
随着我国人口老龄化和居民生活方式的改变, 心血管病已成为威胁我国人民生命和健康的重大 公共卫生问题[1‐2]。为应对不断增长的心血管病负 担,我国已颁布了针对高血压、血脂异常和糖尿病 等心血管病危险因素的各项防治指南[3‐5]。2011年 中华医学会心血管病学分会(CSC)颁布了我国第 一部《中国心血管病预防指南》[6],并于2017年进行 了修订[7]。这些指南的制定和实施对我国心血管 病的防治工作起到了积极的作用。但我国迄今尚 无专门指导心血管病危险因素综合防控的一级预 防指南。2016 年欧洲心脏病学会(ESC)颁布了《2016欧洲心血管病预防临床实践指南》[8],2019年 美国心脏病学学会(ACC)/美国心脏协会(AHA)颁 布了《2019 ACC/AHA 心血管病一级预防指南》[9]。但是由于我国人群心血管病及其危险因素的流行 特征与西方人群有较大差异[10],欧美指南中的一些 建议并不完全适用我国人群。为了从整体上提高 我国心血管病预防能力,努力实现“健康中国 2030”规划纲要的战略目标,达到 2030 年时 4 类重 大慢性非传染性疾病(包括心血管病、肿瘤、糖尿病 和 慢 性 呼 吸 系 统 疾 病)导 致 的 过 早 死 亡 率 较 2015 年降低 30% 的目标,落实预防为主的慢病防控工作方针,由 CSC 牵头,联合中国康复医学会心脏预防与康复专业委员会、中国老年学和老年医学会心脏专业委员会和中国医师协会心血管内科医师分会血栓防治专业委员会,共同制定了《中国心血管病一级预防指南》(以下简称《指南》)。《指南》参考了国内外最新研究结果和相关指南,遵循《中华医学会心血管病学分会关于心血管疾病指南或专家共识制定及文件撰写规范的建议》,坚持科学、公正的原则,形成基于最新临床研究证据的建议文件,用以指导我国心血管病预防实践。
《指南》制定的方法学
一、组织结构
本《指南》的制定过程严格遵循《中华医学会心血管病学分会关于心血管疾病指南或专家共识制定及文件撰写规范的建议》。在CSC指南制定工作组的组织下成立指南制定联合委员会和指南制定工作组,并提名通信作者、主要执笔人及专家委员会成员。专家委员会包括从事临床医学(心内科、内分泌)和公共卫生/预防医学(流行病学、营养学、运动医学等)的专业成员,具有广泛代表性。
二、内容和目标人群
指南编写组一致决定本《指南》的目标人群为尚未发生心血管病临床事件的 18 岁及以上人群。《指南》内容主要聚焦动脉粥样硬化性心血管病(ASCVD)的一级预防。ASCVD指临床明确诊断的动脉粥样硬化性疾病,包括急性冠状动脉综合征、稳定性冠心病、血运重建术后、缺血性心肌病、缺血性卒中、短暂性脑缺血发作、外周动脉粥样硬化疾病等。同时,鉴于我国人群出血性卒中高发的流行病学特征,在血压管理方面也应特别强调评估和控制包括出血性卒中在内的总心血管病风险。其他类型的心血管病,如心力衰竭、心房颤动(房颤)、心脏瓣膜病等不作为本《指南》的主要内容。
三、证据检索和系统评价
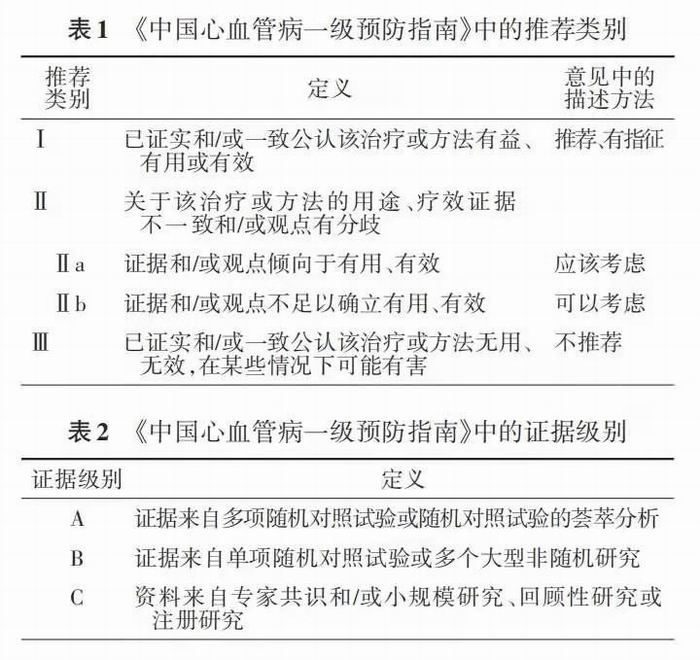
在广泛征集专家意见和多轮讨论后,专家委员会凝练了六大类核心问题,即风险评估、生活方式干预、血脂管理、血压管理、2型糖尿病管理和阿司匹林的使用。主要执笔人首先对这些核心问题进行系统文献检索。如有近期发表的系统综述可直接借鉴,同时注重补充国内研究证据;如无近期发表的系统综述,则需制定检索策略进行系统文献检索,并采用 Newcastle‐Ottawa 量表和 Cochrane 协作网偏倚风险评价工具分别对观察性研究和随机对照试验(RCT)进行研究质量评价。针对尚无发表文献的一些核心问题,指南执笔人直接分析我国人群长期队列研究数据,提供第一手证据。基于上述文献复习和数据分析,同时参考最新国外指南的相关推荐意见,由主要执笔人形成对各核心问题的推荐意见。最后,执笔人和核心专家对有意见分歧的核心问题及其推荐类别(表1)和证据级别(表2)进行讨论,形成共识,以此确定本《指南》各项推荐意见。
四、撰写和审校
指南制定工作组指定的执笔人负责《指南》中心血管病风险评估、生活方式干预、血脂管理、血压管理、2 型糖尿病管理和阿司匹林的使用 6 部分主要内容的撰写。每部分又经过核心专家审校。经执笔人修改后的稿件由专家委员会成员审核通过,然后由通信作者审核通过后正式定稿。
五、其他
《指南》全文和简化版将以书籍、期刊文章、多媒体资料等形式发布,供广大临床医师、公共卫生执业医师和科研人员学习和实践。虽然编写人员付出了极大努力,《指南》可能仍存在不足之处,例如有些推荐意见尚缺乏高级别证据,多数临床试验证据来自国外人群等。
我国心血管病流行病学现状及一级预防面临的挑战
一、我国人群心血管病流行病学现状
公共卫生问题,每年导致死亡人数达 400 万,占总 死亡的 40% 以上,也是伤残和寿命损失的重要原 因。卒中和缺血性心脏病是主要的心血管系统疾 病,分列我国单病种死亡的第一位和第二位[2]。随 着我国人口老龄化和心血管病危险因素水平上升, 心血管病的发病率和死亡率持续升高,以缺血性心 脏病和缺血性卒中为主的ASCVD死亡率升高更为 明显。ASCVD死亡在总心血管病死亡中所占比例 从 1990 年的 40% 上升至 2016 年的 61%,同期年均 死亡人数从 100 万增至 240 万,防治形势日益严 峻[10]。相比之下,我国出血性卒中发病率上升趋势 已基本控制,死亡率明显下降,在总心血管病死亡 中的占比从 1990 年的 39% 下降至 2016 年的 27%。但我国仍是出血性卒中负担最重的国家,出血性卒 中占总心血管事件的 15%~20%,约占所有卒中事 件的 30%[11‐12],是欧美白人的 2~3 倍[13‐14]。可见,我 国人群心血管病的流行病学特征有别于欧美人群, 需要基于国人的研究证据制定适用于我国人群的 心血管病防治策略。
二、我国心血管病一级预防的现状及面临的挑战
1.心血管病一级预防:心血管病的一级预防是 指在心血管事件发生之前,通过控制吸烟、高血压、 血脂异常和糖尿病等心血管病的主要危险因素,降 低心血管临床事件发生风险的预防措施[15]。实践 证明,一级预防措施可有效延缓或避免心血管事件 发生,从而降低心血管病的发病率和死亡率。研究 显示,西方国家心血管病死亡率下降,其中 40%~ 70%归因于危险因素控制[16]。
2.生活方式:健康生活方式是预防心血管病危 险因素发生发展和临床事件的上游措施,是心血管 病预防的基石。根据《中国心血管健康与疾病报告 2019》[1],自 20 世纪 90 年代以来,我国人群的一些 生活方式指标已有改善,但食盐摄入量仍为14.5 g/d, 是我国相关指南推荐摄入量的2倍以上;20岁及以 上人群经常锻炼率为 14.7%,30~39 岁人群只有 12.4%;男性吸烟率高达 50.5%,仍属于全球吸烟率 最高的人群之一。此外,调查显示有 52.7% 的 20~ 34岁吸烟者在20岁以前即每日吸烟。数据提示在 我国不良生活方式仍普遍存在,特别是在青壮年人 群中广泛流行,需大力加强生活方式干预以预防心 血管病。
3.心血管病的危险因素:随着人口老龄化和不良生活方式的流行,具有高血压、血脂异常和糖尿病等危险因素的患者人数快速增加。除需进行生活方式干预外,此类患者大部分需进行药物治疗,增加其对心血管病危险因素的知晓率、治疗率和控制率是心血管病一级预防的关键。
高血压是导致我国居民心血管病发病和死亡 增加的首要且可改变的危险因素,约50%的心血管 病发病和 20% 的心血管病死亡归因于高血压[17]。虽然我国高血压防治已取得长足进步,但最新数据 仍 显 示 我 国 ≥18 岁 成 人 高 血 压 加 权 患 病 率 为 23.2%,估计现患人数2.45亿,而其中仅46.9%的人 知晓,40.7%的人服用降压药,15.3%的人血压得到 控制。特别是 35~44 岁人群高血压患病率已达到 15.0%,但 知 晓 率 、治 疗 率 和 控 制 率 分 别 仅 为 31.7%、24.5% 和 9.9%[18]。此 外 ,在 我 国 有 高 达 23.2% 的 成 年 人 血 压 处 于 130~139/80~89 mmHg (1 mmHg=0.133 kPa)水平,此类中青年人群 15 年 内将有 2/3 发展为高血压,其心血管病发病风险是 血压<130/80 mmHg人群的 3.01倍[19]。可见高血压 的防控力度仍需提高,值得注意的是中青年高血压 人群的早期防治对降低心血管病的长期风险至关 重要。
2000 年以来,我国成人的血脂异常患病率和 患病人数明显增加。2010至2013年的中国居民营 养与健康状况监测研究显示,我国≥18岁人群血脂 异常患病率高达 40.4%[20]。研究显示,在我国人群 中与ASCVD关系最为密切的低密度脂蛋白胆固醇 (LDL‐C)水平显著升高,≥4.14 mmol/L 者达 8.1%,≥ 3.4 mmol/L 者达 26.3%,仅 39% 的人 LDL‐C 处于理 想水平(≤2.6 mmol/L)[21]。然而,目前我国≥18岁人 群血脂异常知晓率、治疗率和控制率仅为 31%、 19.5%和8.9%[22]。
糖尿病不仅是心血管病的独立危险因素,而且 因糖尿病患者一旦发生 ASCVD,其病变弥漫复杂、 预后差,遂近期国内外指南均将糖尿病患者列为心 血管病的高危人群[3,5‐9]。2013 年我国≥18 岁成人 糖尿病患病率为 10.9%,估计患病人数 1.03 亿,是 1980 年的 5 倍,而糖尿病的知晓率和治疗率仅为 36.5% 和 32.2%,在接受治疗的患者中血糖控制率 仅为49.2%[23]。
即使在心血管病高危人群中一级预防的现况也不容乐观。2014至2016年开展的全国七大区域39 个社区的横断面调查显示,在 10 年心血管病风险≥10% 的≥45 岁女性中,降压和调脂治疗率分别为 44.4% 和 10.2%,男性则更低,分别为 36.3% 和6.3%。虽然女性治疗率略优于男性,但控制率却低 于男性[24]。
综上所述,目前我国心血管病发病率和死亡率持续上升。虽然一些不良生活方式的流行和危险因素的防控有所改善,但距离健康中国的目标仍有较大差距,心血管病一级预防面临巨大挑战。倡导全民健康生活方式是预防心血管病的基本策略,同时需进一步规范高血压、血脂异常和糖尿病等危险因素的检出、诊断和治疗,提升其知晓率、治疗率和控制率。生活方式干预和危险因素防控是心血管病一级预防的核心,也是心血管病防控体系的关键。
心血管病一级预防的总体建议
一、概述
《指南》强调对心血管病危险因素的防控应以团队合作为基础,以患者为中心,以医患沟通为手段,充分评估患者的社会相关因素,结合患者意愿,制定合理、有效、可行的个体化干预策略。
二、支持证据
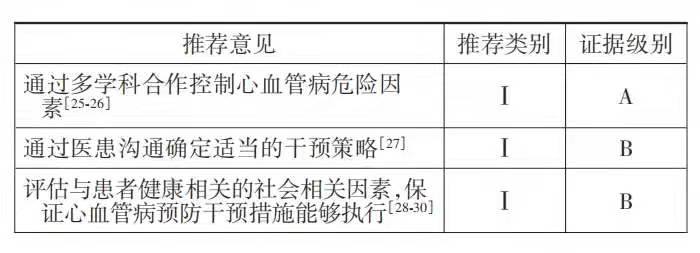
1.通过多学科合作控制心血管病危险因素:以 团队为基础的防治实践是指通过多学科专业人员 的努力以及与患者和家属的合作共同提高心血管 病预防的质量。这种多方合作的实践模式可促进 临床决策制定。既往研究证实,与常规模式相比, 以团队为基础的模式可更好地降低高血压、糖尿病 和血脂异常患者的心血管病风险[25‐26]。
2.通过医患沟通确定适当的干预策略:只有通 过充分的医患沟通才能获得最佳的干预策略。医 师应邀请患者参与针对其本人的个体风险评估,与 患者一起讨论治疗目标及各种干预措施的获益和 风险。患者直接参与临床决策的制定有利于避免 治疗过程中可能遇到的障碍[27]。
3.评估与患者健康相关的社会相关因素:社会 经济状况对危险因素的发生发展和治疗的依从性 都有较大影响,是心血管病发病和死亡风险的重要 决定因素[28]。已有大量观察性研究结果显示,低收入[28]、低教育程度[28]、失业[29]、社区生活环境差[30]等 因素均显著增加心血管病发病风险。因此,临床医 师应通过医患沟通,根据患者的经济状况、教育程 度、文化背景、工作和生活环境等因素来制定最适 合患者的干预措施。
心血管病风险评估
一、概述
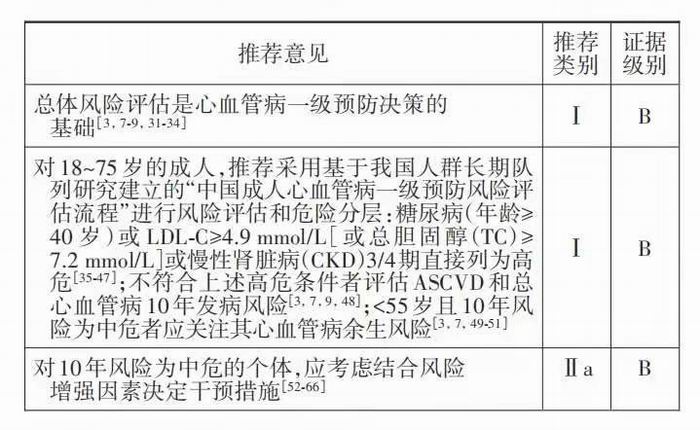
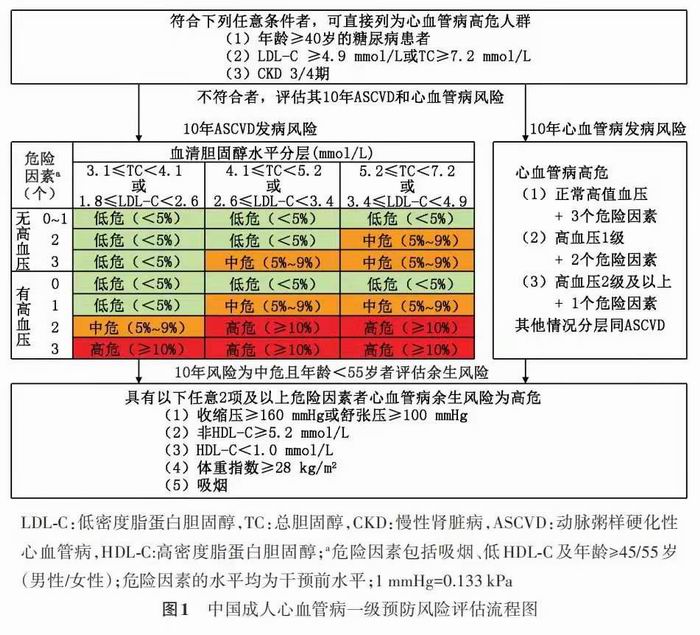
总体风险评估是心血管病一级预防决策的基础。风险评估应在启动干预措施之前进行,依据总体风险评估和危险分层采取不同强度的干预措施是危险因素防控的核心策略(Ⅰ,B)。本《指南》推荐采用基于我国人群长期队列研究数据建立的“中国成人心血管病一级预防风险评估流程(图 1)”评估心血管病风险(Ⅰ,B)。
评估流程分为3步:第一步检出直接列为高危 的个体。糖尿病(≥40 岁)或 LDL‐C≥4.9 mmol/L(或 TC≥7.2 mmol/L)或CKD 3/4期的患者直接列为心血 管病高危人群,无需进行 10 年和余生风险评估。第二步评估10年风险。对于不符合直接列为高危 条件的个体,建议按流程分别评估 ASCVD 和总心 血管病的 10 年发病风险(Ⅰ,B)。10 年 ASCVD 风 险评估延用《中国成人血脂异常防治指南(2016年 修订版)》[3,48] 的方案。该方案将 LDL‐C 或 TC 水平 和高血压作为危险分层的重要参数,同时结合吸 烟 、低 高 密 度 脂 蛋 白 胆 固 醇(HDL‐C)及 年 龄 ≥ 45/55 岁(男性/女性)3 个 ASCVD 危险因素的个数 分成21种组合,并按照不同组合的10年ASCVD发 病平均风险按<5%、5%~9% 和≥10% 分别定义为低 危、中危和高危。<40 岁的糖尿病患者较为年轻、 病程较短、糖尿病本身相关的ASCVD风险不高,应 结合其他危险因素评估其 10 年 ASCVD 风险和余 生风险。10 年 ASCVD 风险分层主要用于指导调脂、降糖治疗以及阿司匹林的使用(阿司匹林的使用需结合表 3 中的风险增强因素,详见“阿司匹林的使用”部分),而在决定降压治疗策略时,还需考虑包括ASCVD和出血性卒中在内的总心血管病风险(详见“血压管理”部分)。血压为正常高值[130~139/85~89 mmHg]且合并吸烟、低 HDL‐C 及年龄≥45/55岁(男性/女性)3个危险因素,高血压1级合并上述危险因素中的 2 个,或高血压 2 级合并上述危险因素中 1 个时,总心血管病的 10 年发病风险≥10%,为高危。其他情况下总心血管病风险分层与ASCVD 的风险分层一致。第三步评估余生风险。10 年心血管病发病风险为中危且年龄<55 岁的人群应进行心血管病余生(终生)风险的评估,以识别中青年群体中心血管病余生风险高危的个体。具有以下任意 2 个或以上危险因素者心血管病余生风险为高危:(1)收缩压≥160 mmHg 或舒张压≥100 mmHg;(2)非 HDL‐C≥5.2 mmol/L(200 mg/dl);(3)HDL‐C<1.0 mmo/L(40 mg/dl);(4)体 重 指 数(BMI)≥28 kg/m2;(5)吸烟。
需指出,上述危险分层仅考虑了主要伴随疾病的状态和危险因素,而在临床实践中每位患者的实际情况可能更为复杂,医患双方往往需针对风险充分讨论。如对于风险评估为中危的人群,是否启动他汀类药物治疗有时难以确定。此外,考虑一级预防时是否使用阿司匹林,仅依据ASCVD10年风险≥10%尚不足以识别获益显著大于风 险 的 人 群[67]。上 述 情 况 下 可 考 虑 结 合 心 血 管 病 风 险 增 强 因 素 (表 3)[52-57,65-66,68-74],在充分考虑患者 意愿的前提下进一步确定是否启动 干预措施(Ⅱa,B)。
二、支持证据
1.总体风险评估是心血管病一 级预防决策的基础:心血管病是多 个危险因素共同作用的结果,心血 管病风险不仅取决于某一危险因素 水平,还取决于多个危险因素的相 互作用[37],而多重危险因素共同干 预可能具有协同作用,有助于进一 步降低心血管病风险[75]。因此,孤 立控制单一危险因素是不够的,应 重视对心血管病总体风险的综合评 估。心血管病总体风险评估指根据 心血管病多种危险因素的水平和组 合判断或预测一个人或一群人未来(5 年、10 年或 余生)发生心血管病急性事件的概率”[76]。总体风 险评估是心血管病一级预防决策的基础(Ⅰ,B)。国内外多部心血管病预防和危险因素防控指南推 荐根据个体的心血管病总体危险分层决定干预的 起始和目标水平,对不同的风险等级给予相应强度 的干预,从而最大程度提高预期效益,避免过度治 疗可能造成的危害,同时优化医疗资源配置、节约 医疗费用[3,7‐9,31‐34]。
2.风险评估的流程:心血管病风险评估需基于 由长期随访数据的队列研究建立的数学模型。国 际上广泛使用的预测模型包括美国弗莱明翰心脏 研究模型、欧洲的 SCORE 模型和美国的汇总队列 模型等[76]。然而,既往研究显示上述基于欧美人群 数据建立的预测模型并不适用于我国人群[77‐79]。为此,我国学者基于国内心血管病队列研究的长期 随访数据建立了冠心病[77]、卒中[80]、缺血性心血管 病[11,78]、ASCVD[48] 和总心血管病[79]的 10 年发病风 险预测模型。为保持风险评估方案的延续性,本指 南采纳《中国成人血脂异常防治指南(2016年修订 版)》[3,48]的 10年 ASCVD发病风险评估方案作为调 脂治疗、降糖治疗和阿司匹林干预的决策依据;同 时评估包括ASCVD和出血性卒中的总心血管病风 险,以便检出总心血管病高危个体,更好地指导与 出血性卒中密切相关的降压治疗决策。
风险评估的第一步是检出心血管病高危个体, 包括≥40 岁的糖尿病患者或 LDL‐C(或 TC)水平极 高或 CKD 3/4 期的患者。大量观察性研究及荟萃 分析显示糖尿病患者心血管病发病风险显著升 高[35‐36]。虽然也有研究显示糖尿病患者的心血管 病风险不足以等同于已患有心血管病的患者[81],但 糖尿病患者常合并多种心血管病危险因素[37],其 ASCVD 病变更为严重[82],长期心血管病风险较 高[38],且一旦发生心血管事件预后更差[39]。此外, 多项 RCT 及荟萃分析结果显示他汀类药物治疗可 降低40~75岁糖尿病患者ASCVD风险[40]。LDL‐C≥ 4.9 mmol/L(或 TC≥7.2 mmol/L)的严重高胆固醇血 症患者 ASCVD 发病风险显著升高,可能存在家族 性高胆固醇血症(familial hypercholesterolemia,FH) 等遗传异常及高胆固醇水平的长期暴露,从而导致 极高的早发 ASCVD 风险[41‐43]。越来越多的证据显 示强化降胆固醇治疗可显著降低此类患者 ASCVD 风险[44‐45]。此外,还有大量队列研究及荟萃分析显 示 估 算 的 肾 小 球 滤 过 率(estimated glomerular filtration rate,eGFR)降低者心血管病风险增加, eGFR<15 ml·min-1·1.73 m-2 者心血管病风险增加 2倍以上,且独立于传统危险因素[46‐47]。因此,参考 国内外相关指南[3,7‐9],建议将糖尿病(年龄≥40 岁) 或LDL‐C≥4.9 mmol/L(或TC≥7.2 mmol/L)或CKD 3/4期 的患者直接列为心血管病高危人群,并应积极进行 干预,无需再进行10年和余生风险评估。
风险评估的第二步是对于不符合上述高危条件人群,按本《指南》建议的流程评估 ASCVD 和总心血管病 10 年发病风险。10 年 ASCVD 发病风险 评估延用《中国成人血脂异常防治指南(2016年修 订版)》的方案[3]。该方案以中国多省市心血管病 队列研究长期随访建立的预测模型为基础。经验 证,该模型具有较好的判别和校准能力[48]。此外, 虽然 ASCVD 已成为我国人群的主要心血管病类 型,但出血性卒中仍占心血管病发病的近20%和心 血管病死亡的近 30%[10‐12]。因此,我国人群心血管 病一级预防需同时考虑ASCVD的风险和包括出血 性卒中在内的总心血管病风险。
风险评估的第三步是对<55 岁且 10 年心血管 病发病风险为中危的人群进行余生风险评估。年 龄是预测10年心血管病发病风险最重要的危险因 素,中青年人群即使合并 3 种心血管病危险因素, 其 10 年心血管病风险仍可能达不到高危,而危险 因素的累积暴露可能增加长期心血管病风险。如 仅依据 10 年风险评估结果,可能错失早期预防的 契机,因此提出了心血管病余生风险的概念[83]。余 生风险也被称为终生风险,指被观察个体在其平均 期望寿命内发生目标事件的绝对累积风险。目前, 美国、日本等已有心血管病余生风险的研究报 道[84‐85],我国队列研究也相继发布了中国人群心血 管病余生风险的研究结果[49‐50]。经模型预测,对于 余生风险高危个体进行早期干预,可避免或延迟心 血管病的发生,获得更长的无事件预期寿命,终生 获益更多[51]。近年来,心血管病余生风险评估陆续 被引入到欧美及中国的心血管病防治指南,作为心 血管病 10 年风险评估的补充。本《指南》沿用《中 国成人血脂异常防治指南(2016年修订版)》[3] 的余 生风险评估方案。心血管病余生风险评估为中青 年人群的风险管理提供了依据,对于激励个体改善 生活方式和提高治疗依从性意义重大。
3.心血管病风险增强因素:对于高危个体应积 极进行干预,通常需在生活方式干预的基础上启动 药物治疗。对于低危个体则建议保持健康生活方 式,定期进行危险因素筛查。对于 10 年风险为中 危的个体,预防干预的利弊不明确,是否需启动药 物治疗有时难以决断。风险评估为中危,即传统危 险 因 素 某 种 组 合 下 的 平 均 预 测 风 险 处 于 5%~<10%,而实际情况下各种危险因素水平的高 低及合并的其他因素可能使个体风险高于或低于 预测水平。除传统心血管病危险因素外,大量研究 发现还有很多靶器官损害的指标[53‐54,58‐60,65‐66]、血清 生物标志物[52,54‐57] 以及心血管病家族史、先兆子痫、风湿性关节炎[9,61] 等因素与心血管病密切相关。但研究显示在加入预测模型后,踝/臂血压指数 (ABI)[54]、颈总动脉内膜中层厚度(IMT)[62]、FH[54]、 高敏 C 反应蛋白(hsCRP)[54] 以及非 HDL‐C、甘油三 酯(TG)和载脂蛋白 B(ApoB)[55] 等指标未能在传统 危险因素的基础上改善模型的预测能力或危险分 层。冠状动脉钙化(CAC)、颈动脉 IMT 和斑块、 ABI、ApoB、脂 蛋 白 a[lipoprotein(a),Lp(a)]和 hsCRP 等指标尚不能普遍在基层医疗机构进行检 测且费效比还有待评价。因此,目前国内外心血管 病风险评估模型纳入的因素均以传统心血管病危 险因素为主[76]。那些与心血管病密切相关但尚不 宜纳入预测模型的因素可作为心血管病风险增强 因素,当 10 年风险评估为中危的个体难以权衡治 疗的风险与获益时,建议考虑结合上述风险增强因 素确定是否启动干预措施(Ⅱa,B)。所具有的风险 增强因素越多越倾向于高危,反之亦然。值得注意 的是 CAC 积分为 0 时,绝大多数患者 10 年 ASCVD 风险<5%[63],可暂不考虑药物干预[64]。
生活方式干预
一、合理膳食
(一)概述
合理膳食包括增加新鲜蔬菜、全谷物、粗杂粮等纤维摄入,减少饱和脂肪,减少烹饪、调味品用盐(包括食盐、酱油及酱制品),控制胆固醇、碳水化合物摄入、避免摄入反式脂肪等措施,有助于逆转或减轻肥胖、高胆固醇血症、糖尿病和高血压以及心血管病预防。但既往包含心血管结局的RCT有限,证据多来自观察性研究。多项研究关注了饮食模式与心血管病死亡率的关系,特别是糖、低热量甜味剂、高碳水化合物饮食、低碳水化合物饮食、精制 谷物、反式脂肪、饱和脂肪、钠(盐)、红肉(通常指 猪、牛、羊肉等)和加工红肉制品(如培根、腊肠、火 腿等)方面的研究[86‐99,106‐108,110‐117]。
中国营养学会建议的“中国居民平衡膳食”模 式强调食物多样化,并注意能量平衡,每日摄入大 米、小麦、玉米、马铃薯等谷薯类食物250~400 g(其 中全谷物和杂豆类 50~150 g、薯类 50~100 g),蔬菜 300~500 g,水果 200~350 g,鱼、禽、蛋、瘦肉 120~ 200 g(其中蛋类 40~50 g,相当于 1 个鸡蛋),奶类 300 g。合理膳食可增加纤维素、维生素、钾等摄入 量,降低血脂、改善心血管健康[118]。膳食结构及主 要食物来源见表4。
(二)支持证据
1.健康膳食结构有助于降低心血管病风险:观 察性研究结果显示,摄入以植物为基础的素食加之 水果、坚果、蔬菜、豆类、低脂的植物或动物蛋白(最 好是鱼类)、固有可溶性和不溶性植物纤维以及地 中海饮食(主要由全谷物、坚果、蔬菜和水果组成并 辅以橄榄油、鱼类和红酒等,包括较少的家禽和奶 制 品 、红 肉 和 肉 制 品)的 人 群 全 因 死 亡 率 较 低[86‐89,91‐92,94,119‐120]。PREDIMED 研究结果显示地中 海饮食加之特级初榨橄榄油或坚果可降低人群复 合终点事件(心肌梗死、卒中或心血管病死亡)的发 生率,其中以减少卒中为主[86]。进一步分析显示, 植物源性食物占比最高的“超素食”饮食模式可显 著降低人群死亡率[96]。CARDIVEG 研究将超重的 受试者分为低卡路里素食组和地中海饮食组,并进 行交叉研究,结果发现2种饮食模式均能有效降低 体重、BMI 和脂肪量,其中素食降低 LDL‐C 更为有 效 ,而 地 中 海 饮 食 降 低 TG 水 平 更 为 有 效[113]。Adventist Health Study‐2 队列研究表明,动物蛋白 高摄入者较低摄入者死亡率增加61%;而用坚果和 种子类食物代替肉类作为蛋白质来源,其高摄入者较低摄入者死亡率降低 40%[95]。芬兰的一项男性 队列研究结果显示饮食中动物蛋白比例高、肉类摄 入量大者死亡风险高[114]。一项针对美国医疗保健 专业人员的前瞻性队列研究结果显示用植物蛋白 替代动物蛋白可减少心血管病死亡率,与植物蛋白 相比,摄入家禽和鱼类、乳制品、未加工红肉、鸡蛋、 加工红肉者死亡率分别增加 6%、8%、12%、19%、 34%。总体而言,植物蛋白每增加 3% 的能量替代 动物蛋白死亡率降低 10%[94]。关于摄入乳制品以 减少ASCVD风险因素有效性的证据不一。包括低 脂 乳 制 品 的 DASH[dietary approaches to stop hypertension(膳食途径终止高血压)]饮食可降低血 压[103]。PURE研究结果显示,与无乳制品摄入者比 较,每日摄入乳制品 2份(约 500 ml)心血管死亡率 降低 23%[121]。但上述美国医疗保健人员的队列研 究结果显示,与摄入植物蛋白相比,摄入乳制品心 血管死亡率增加11%[94]。
2. 胆固醇与 ASCVD 风险:膳食中胆固醇的来 源包括肉类、鸡蛋等。其中肉类(包括家禽、红肉、 加工肉制品及海鲜)对胆固醇贡献约占 42%,鸡蛋 约占 25%,其他约占 1/3。目前膳食胆固醇摄入与 心血管病及死亡之间的关系仍具有争议。由于混 杂因素较多,观察性研究的结果不一,通常不支持 饮食中胆固醇与心血管病风险存在关联;但干预研 究及荟萃分析的结果提示高胆固醇摄入可导致血 TC、LDL‐C水平升高[122]。20多年来,我国居民膳食 胆固醇摄入量上升34%,目前成人平均摄入量已达 266.3 mg/d,与美国相当,且其中 1/3 每日胆固醇摄 入量已经超过既往推荐的300 mg的界限[123]。尽管 目前多数指南因证据不足取消这一界限,但过高的 胆固醇摄入导致血胆固醇水平升高带来的潜在风 险仍不容忽视。2019 年美国 AHA 给出如下建议 (供参考):在遵循当前健康膳食模式的基础上,普 通人每日食用1个鸡蛋(585 mg胆固醇/100 g鸡蛋) 或等量胆固醇;素食者如无其他胆固醇来源,可适 当增加奶制品及蛋摄入量;高脂血症的患者,尤其 是 2 型糖尿病或心力衰竭高风险人群摄食高胆固 醇食物需谨慎;非高胆固醇血症的老年人可适当增 加鸡蛋摄入,不超过每日2个[124]。
3.饱和脂肪、不饱和脂肪与 ASCVD风险:反式 脂肪和饱和脂肪与总死亡风险增加及特定原因的 死亡相关,用不饱和脂肪酸等效替代 5% 的饱和脂 肪总死亡率可降低 27%[97]。而 PURE 研究的结果 显示,使用饱和脂肪和不饱和脂肪替代精制碳水化合物可减少卒中发生、降低死亡率[98]。
4. 反式脂肪(酸)与 ASCVD 风险:摄入反式脂 肪(酸)可增加ASCVD风险。研究表明反式脂肪与 高全因死亡率有关[97,99]。一些食品添加剂含部分 (未完全)氢化油,是反式脂肪酸的来源[102]。研究 发现在食品工业中禁止使用反式脂肪的法规与卒 中和心肌梗死的减少有关[100]。反式脂肪对脂质和 脂蛋白有不利影响,并可加剧内皮功能障碍、胰岛 素抵抗、炎症和心律失常[125]。
5. 盐与心血管病风险:DASH 研究和 TOHP 研 究结果显示减少日常钠摄入量可降低血压和心血 管 事 件 发 生 率[103,115‐116]。国 家 健 康 与 营 养 调 查 (National Health and Nutrition Examination Surveys, NHANES)的数据表明,摄入过多钠[>2 g/d(相当于 5 g食盐)]与心血管死亡相关[105]。一项关于山东省 多区县钠摄入量与心血管病死亡的调查分析显示, 2011 年山东省 25~69 岁人群中近 20% 的心血管死 亡可归因于高钠摄入(>2 g/d)引起的收缩压升 高[126]。世界卫生组织(WHO)全球慢病防控目标为 到 2025年人群钠摄入量应较 2010年减少 30%[127]。2012年我国居民膳食钠摄入量(5 702 mg/每标准人 日,折合成食盐的量为14.5 g)仍然远高于推荐的摄 入量(中国推荐<6 g/d,WHO 推荐<5 g/d)[1]。通过 减少烹调用盐以及避免高盐食物等措施有助于降 低血压、减少 ASCVD 发生风险。而 PURE 研究对 限盐提出了挑战,研究显示 WHO 推荐的低钠摄入 (<2 g/d)和高钾摄入(>3.5 g/d)在其研究人群中非 常罕见(仅为 0.002%),适量的钠摄入(3~5 g/d)与 高钾摄入相结合,死亡和心血管事件的风险最 低[117]。这一结果有待更多证据支持。此外,我国 成人钾摄入量普遍低于WHO和中国营养学会推荐 的水平。因此鼓励增加蔬菜、水果等天然富含钾的 食物的摄入,可能有助于预防心血管病。
6. 碳水化合物与 ASCVD 风险:高碳水化合物 (糖)摄入可能增加 ASCVD 风险。每日饮用 1份含 糖饮料可使患糖尿病的几率增加 20%[106]。研究显 示每日摄入的添加糖的能量超过全天能量的 10% 与死亡率增加有关[107]。习惯摄入高糖饮料的成人 可采用低卡路里甜味饮料作为替代,提供甜味的同 时减少热量摄入,并有能利于向纯水过渡[108]。REGARDS研究显示,美国南方饮食模式(包括较多 的油炸食品、内脏、加工肉类及甜味饮料)显著增加 健康风险,其中冠心病风险增加 56%,卒中风险增 加 30%[109]。食 用 果 汁 、含 糖 饮 料 、精 制 谷 物 、土豆/薯条和甜食会增加冠状动脉事件发生率,甚 至比食用动物制品的风险还高[89]。此外,长期低碳 水化合物但高动物脂肪、蛋白质摄入的饮食模式与 心脏和非心脏死亡率增加相关[110‐112]。ARIC研究显 示,含动物源性蛋白质和脂肪(如羊肉、牛肉、猪肉、 鸡肉)的低碳水化合物饮食与死亡率增加相关,而 植物源性(如蔬菜、坚果、花生酱、全麦面包)与死亡 率降低相关;包含 ARIC 的队列研究的荟萃分析结 果显示,高碳水化合物摄入(供能>70%)及低碳水 化合物摄入(供能<40%)均增加死亡风险,供能占 50%~55%定义为适度的碳水化合物摄入[110]。中国 健康与营养调查的数据表明,高碳水化合物饮食可 能与心血管病的危险因素有关,建议每天摄入适量 的碳水化合物[128]。此外,饮用添加人工甜味剂的 饮料增加卒中、冠心病及全因死亡风险[129],应避免 饮用。
二、身体活动
(一)概述
规律身体活动是维持和改善心血管健康的基 石[133]。2014年国民体质监测结果显示 20~59岁人 群身体活动达标率仅为22.8%[139],仅为同期美国人 群身体活动达标率的一半[140]。而中国健康与营养 调查显示,1991 至 2011 年中国居民身体活动量呈 下 降 趋 势[1] 。因 此 ,需 大 力 提 倡 增 加 身 体 活动[141‐142]。
观察性研究的荟萃分析和系统综述支持加强 有氧运动以降低 ASCVD 风险的建议[130‐135,143]。有 氧运动通常是安全的[144],可以采用快走、慢跑、游 泳、骑自行车、广场舞等形式。但习惯于久坐不动 的人开始进行身体活动时应从低强度、短时间开 始,循序渐进[145]。目前尚不明确长期达到活动量 或强度上限是否会对心血管产生不良后果[146]。需 与患者进行沟通,高强度的身体活动仅适用于小部 分人群[140]。老年人也可选择瑜伽、太极拳、广场舞 等形式进行活动,以增加心肺适应性。对于已存在明显功能障碍的患者,身体活动的形式、强度和时间需结合患者情况给与个体化指导。
抗阻运动(如健身器械、弹力带等)可改善身体 机能[143]、有助于糖尿病患者的血糖控制[147‐148] 并降 低血压[149]。但尚不清楚抗阻运动能否降低心血管 病风险[140]。
静态生活方式对健康有害。尽量减少久坐时 间,可能有助于降低心血管病风险[130,136‐138]。
关于身体活动的强度有多种评价方式。以代谢当量(metabolic equivalent,MET)为例,MET 指相对于安静休息时身体活动的能量代谢水平,表现为单位时间能量消耗量。1 MET相当于每公斤体重每分钟消耗 3.5 ml 氧,或每公斤体重每小时消耗1 kcal(1 kcal=4.184 kJ)能量的活动强度。低、中、高强度身体活动对应的通常为1~<3、3~<6、≥6 MET。
(二)支持证据
1.中高强度身体活动降低心血管病风险:众多 研究一致显示中至高强度身体活动与心血管事件 和死亡减少相关[130‐135]。我国一项大型前瞻性队列 研究表明,无论是职业性还是非职业性身体活动均 与心血管病风险呈负相关,即活动量越大心血管病 风险越低。每日 4 MET 或更高强度的身体活动可 使各种心血管病风险降低 5%~12%[150]。建议成人 每周应进行至少 150 min 中等强度身体活动或 75 min 高强度身体活动两种方式结合。有证据显 示更高强度的身体活动,如每周累计进行 300 min 以上的中等或 150 min 以上的高强度身体活动,心 血管病风险进一步下降;进一步增加身体活动达到 极 高 水 平 ,会 带 来 持 续 但 逐 渐 减 少 的 附 加 效 益[132‐133,140],但其潜在风险不明确,不做常规推荐。
2.规律的身体活动有助于降低心血管病风险:中至高强度的身体活动一旦开始,降低 ASCVD 风 险的收益即出现并逐渐增加[133]。研究表明即使活 动水平低于当前的推荐量,心血管保护效果依然明 显[151‐152]。因而鼓励所有成年人达到建议的最低活 动量,不能达到最低标准者应循序渐进、量力而行, 选择适宜的活动强度与时间,以最大程度地降低心 血管病风险[133]。
3. 减少久坐等静态生活方式有助于降低心血 管病风险:久坐行为指在清醒状态下长时间坐位不 活动,能量消耗通常≤1.5 MET[153]。久坐行为与心 脏代谢危险因素增加相关[130,136‐138]。平时很少进行中至高等强度身体活动的人,久坐可能大大增加心 血管病风险[130,137]。因此减少久坐行为,特别是未达到当前推荐身体活动水平者,可能有助于降低心 血管病风险[154]。
三、控制体重
(一)概述
近年来我国成人中超重及肥胖者所占比例呈 上升趋势,农村居民超重和肥胖率虽低于城市居民 但上升幅度超过城市居民[1]。
肥胖及超重人群心血管病风险增加[157‐162]。大量 研究发现通过限制热量摄入、增加身体活动等方式 减轻并维持体重,有助于降低心血管病风险,甚至可 减少全因死亡[155‐156]。而单纯采用药物干预虽也可减轻并维持体重,但不良反应率高且难以坚持[155]。近 年来,对于重度肥胖者,可通过胃减容手术减重取得 一定效果,但在一级预防中尚难普及[163]。
(二)支持证据
LeBlanc等[155] 关于127项RCT荟萃分析的结果显 示,限制热量摄入、增加身体活动等行为模式改变坚 持12~18个月,可有效减轻并维持体重,可降低血压以 及LDL‐C和血糖水平,减少新发糖尿病且不增加其他心血管病风险。采用药物治疗12~18个月,同样可有效减轻并维持体重,但由于药物的不良反应,患者往往难以坚持。Ma等[156] 对纳入共30 296名受试者的 54项RCT进行了荟萃分析,发现低脂肪及低饱和脂肪饮食联合或不联合身体活动减重,可使全因死亡风险下降18%,心血管病死亡风险下降7%。推荐将每周 150 min以上中等强度有氧运动作为初始减重措施, 每周200~300 min高强度身体活动用于维持体重、减少反弹。热量摄入男性宜控制在1 500~1 800 kcal/d, 女性则为1 200~1 500 kcal/d。极低热量(<800 kcal/d) 摄入需在专业人员指导下进行,不建议常规采用[164]。上述行为模式改变,可以在6~12个月内使体重下降 5%~10%,平均约8 kg,随后虽略有反弹,但仍可见其 他心血管病危险因素的持续改善[155‐156]。
四、戒烟
(一)概述
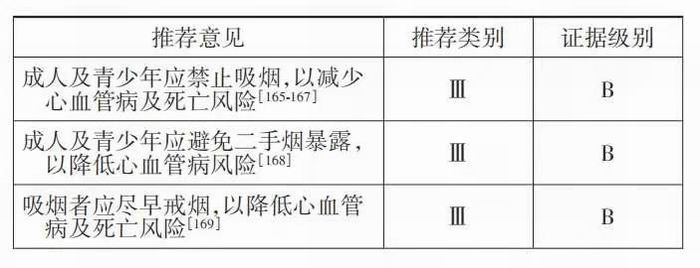
吸烟有害健康。大量观察性研究显示,吸烟及二 手烟暴露与心血管病、肺癌或慢性呼吸道疾病、肝癌 及其他肿瘤发病及风险直接相关[170]。队列研究显示, 戒烟者发病和死亡风险显著低于持续吸烟者。吸烟 者无论何时戒烟都会获益。越早戒烟,获益越多[171]。
我国是吸烟人数最多的国家。吸烟带来的疾 病负担和经济损失巨大[172]。戒烟是预防心血管病 及其他慢性病的重要措施。避免吸烟及二手烟暴 露,应从青少年开始[167‐168]。戒烟5年后心血管病风 险可恢复正常水平。
帮助吸烟者戒烟对于预防与控制心血管病非 常重要。医护人员应帮助吸烟者了解吸烟的危害, 提高戒烟意愿,提供戒烟帮助并安排随访。对于烟 草依赖者,应评估其依赖程度并进行治疗,提供简 单的戒烟方法,必要时进行药物治疗[173‐174]。同时 邀请吸烟者的家人、朋友参与戒烟计划,建立一个 良性的支持环境[175‐176]。
2015年我国男医师吸烟率为43.0%,医务人员 不应吸烟,吸烟者应及早戒烟,应发挥健康示范作 用。应注重宣传和落实公共场所禁烟。医疗机构 应率先成为无烟场所。除帮助患者戒烟外,更应督促并支持各级政府制定公共场所、公共交通工具及 办公场所有效控烟的法规,为公众创造无烟环境, 宣传吸烟的危害[175‐176]。研究显示,医务人员在日 常诊疗中对儿童和青少年进行防止吸烟和戒烟干 预有助于青少年认识吸烟的危害、帮助吸烟者遵照 方案戒烟[175]。
(二)支持证据
1.吸烟增加心血管病及死亡风险:吸烟是心血 管病及死亡的独立危险因素,且吸烟量越大、时间 越长心血管病发病及死亡风险越高[165‐167]。调查还 发现,即便调整其他危险因素,年轻人吸烟仍与心 血管病密切相关[167]。因而提倡青少年远离烟草。
2.二手烟暴露增加心血管病风险:二手烟暴露 同样增加冠心病、卒中等心血管病风险[168‐170]。研究 显示不吸烟者暴露于二手烟其冠心病及卒中风险增 加20%~30%[170]。青少年也应避免二手烟暴露。
3.戒烟的获益:戒烟可降低心血管病的发病与 死亡风险[166]。戒烟1年后,冠心病患者死亡及再发 心脏事件的比率即可下降 50%[169],心肌梗死患者 死亡率可降低70%以上[177];戒烟15年后,冠心病和 心力衰竭患者的死亡风险与从不吸烟者相似[169]。应使吸烟者认识到戒烟的益处并积极鼓励其戒烟。
五、控制酒精摄入
高血压、糖尿病、房颤、肝肾功能受损者以及孕 妇和青少年不建议饮酒。普通人群也不建议通过 少量饮酒来预防心血管病。
(二)支持证据
过量饮酒增加心血管病及死亡风险。全球每 年因长期过量饮酒或偶尔大量饮酒导致的死亡人数 高达300万。过量饮酒可导致肝硬化、肿瘤及交通 事故,并增加房颤、心肌梗死及心力衰竭风险[178‐179]。还有研究显示饮酒量与高血压、房颤及出血性卒中 密切相关[178]。不同种类的酒与心血管病风险的关 系不完全相同。对观察性研究的荟萃分析显示,红 酒、啤酒与心血管事件间存在J形曲线关系,即适量 时血管事件风险最低,过量时风险增加;而烈性酒与 血管事件风险间未见 J 形曲线关系[181]。一项关于 83项前瞻性研究、超过50万饮酒者的分析显示,每 周酒精摄入100 g以下者死亡风险最低,在此之上随 饮酒量增加无基础心血管病史者其卒中、心肌梗死、 心力衰竭、致死性高血压疾病及主动脉瘤发生率逐 渐增加,以每周酒精摄入量≤100 g为参照,40岁以上 成人随着每周饮酒量倍增预期寿命缩短6个月或更 多 ,提 示 饮 酒 量 低 于 当 前 推 荐 的 标 准 可 能 更 安全[184]。
六、保持健康睡眠
(一)概述
睡眠与心血管病风险密切相关。健康睡眠包括充足的时间和良好的质量。大量观察性研究及荟萃分析结果显示失眠与心血管病发病率和死亡率增加相关。睡眠时间过短增加高血压、冠心病及心力衰竭的风险,而每日保持 7~8 h充足的睡眠时间 及 良 好 质 量 的 人 群 心 血 管 病 风 险 明 显 降低[186,188‐193]。
(二)支持证据
挪威及中国台湾地区随访 10年以上的队列研 究显示失眠增加心肌梗死、卒中的发生风险[191‐192], 心力衰竭的发生率也明显增加[193]。此外,荟萃分析 还发现失眠者心血管病死亡风险显著增加[190]。荷 兰一项前瞻性队列研究纳入 17 887 名基线无心血 管病的健康受试者并随访12年,发现每日睡眠不足 6 h者比7~8 h者心血管病风险增加15%,冠心病风 险增加23%;此外,在健康饮食、规律身体活动、不吸 烟等良好生活方式的基础上,睡眠时间充分、质量好 的健康睡眠者相比睡眠不足、质量差者,包括心肌梗 死、卒中及心血管死亡在内的复合心血管事件风险 减少65%,心血管死亡风险降低83%[188]。
七、保持良好的心理状态
血压管理
一、有助于降低血压的生活方式
(一)概述
国家“十二五”中国重要心血管病患病率调查 及关键技术研究显示,男性、高龄、超重/肥胖、高血 压家族史、教育程度低、吸烟和饮酒与高血压风险 增加有关[18]。
生活方式干预在任何时候对任何高血压患者 (包括正常高值者和需药物治疗的高血压患者)都 是合理、有效的,目的是降低血压和控制其他危险 因素。干预包括合理膳食、限盐、限酒、减重和身体 活动。
(二)支持证据
1.合理膳食:研究显示 DASH 饮食可使高血压 患 者 收 缩 压 降 低 11.4 mmHg、舒 张 压 降 低 5.5 mmHg,一 般 人 群 可 分 别 降 低 6.7 和 3.5 mmHg[204]。DASH 饮食可有效降低冠心病和卒 中风险[205‐206]。目前我国尚缺乏对高血压患者全按 照DASH饮食进行干预的研究,评估饮食依从性的 方法也有很大差异性[226]。但研究发现对 DASH 饮 食、中国膳食宝塔和替代性健康饮食依从性高的人 群高血压发病率较低[227],另外其总死亡、心血管事 件和糖尿病的发生率均较低[207‐208]。一项纳入85例 妊娠高血压患者的RCT中,41例进行DASH饮食的 患者子痫前期、早产和低出生体重儿的发生率均明 显降低[209]。
2.减盐:2010年全球人均钠摄入量为3.95 g/d, 有 165 万人死于钠摄入增加导致的心血管病[210]。高钠、低钾膳食是我国人群重要的高血压发病危险 因素。限制钠盐的摄入对不同种族人群均有降压 作用,对亚裔人群更为显著[228]。观察性研究也显 示虽在其他国家人群中随钠摄入增加卒中发病减 少,但在中国人群中二者仍然呈正相关[211]。
血压升高个体更需限制钠盐摄入,每日食盐 (氯化钠)摄入应逐渐减少至小于5 g。除减少烹饪 添加食盐外,还要减少使用含钠的调味品(酱油、味 精、鱼露等)。另外,少吃加工类食物(糕点、火腿、 罐头等)。推荐多吃蔬菜、水果、低脂乳制品、鱼、全 谷类、纤维类、富含钾和其他矿物质的食物。
3.控制体重:超重和肥胖人群减重5%~10%可 降低血压,且随体重降低幅度增加血压进一步下 降[212],并可提高血压达标率[213],减少服用降压药的 种类[214]。然而长期减重(6 个月以上)治疗的依从 性明显降低,血压可随体重反弹而上升[229‐230]。超 重、肥胖的高血压及正常高值血压人群,减重均 具 有 明 显 的 降 压 作 用 ,在 高 血 压 患 者(血 压 >140/90 mmHg)和接受降压药物治疗的人群血压降 低幅度更大[215]。
中国一队列研究显示,年龄大、基线超重或肥 胖 的 中 老 年 人 群 体 重 变 化 导 致 血 压 的 变 化 更 大[216],提示此类人群需更积极地控制体重。
对于不能通过改善生活方式减重的肥胖患者, 胃部环缩术可显著降低体重和血压[231],但减重药 物的降压作用非常有限[232‐233]。建议通过减重,使 BMI<24 kg/m2,腰围<90/85 cm(男性/女性)。
4. 身体活动:身体活动可改善血压水平。研 究显示,对于平均血压为 147/92 mmHg 中年高血 压人群,通过规律的有氧运动(快步走、慢跑、骑自 行车,每周 3~5次,每次 30~60 min),可使血压降低 6.1/3.0 mmHg[217]。有 氧 运 动 可 使 收 缩 压 降 低 3.84 mmHg,舒张压降低 2.58 mmHg,高血压和正常 血压人群均可获益[218]。队列研究发现,高血压患 者定期进行身体活动其心血管和全因死亡风险均 降低[219]。
对于高血压患者,抗阻运动可显著降低舒张 压,但对收缩压作用较弱[234]。坚持等长阻力训练 (平板撑、靠墙蹲、臀桥等)8周以上,可获得显著的 降压效果,尤其是45岁以上的男性高血压患者[235]。有氧运动与抗阻运动结合与单纯的有氧运动比较, 组间血压变化差异无统计学意义[236],需注意高血 压患者应慎重进行高强度有氧运动[237]。
血压变化取决于每次身体活动的时间和频 率[238]。对于老年患者,低中强度身体活动12周,对 血管弹性改善作用明显[220],高龄老年高血压患者 进行有氧运动(每周 2~3 次,每次 20~30 min)还有 助于降低收缩压[221]。
因此,无论高血压还是非高血压人群均建议除 日常生活活动外,进行每周 4~7 d、每日累计 30~ 60 min 的中等强度身体活动,可采取有氧、抗阻和 伸展等形式,应以有氧运动为主、无氧运动作为补 充。适宜的身体活动强度须因人而异,常用活动时 最大心率评估适宜中等强度身体活动。中等强度 身体活动即活动时心率达到最大心率的 60%~ 70%,最大心率(次/min)= 220-年龄。高危患者活 动前须接受评估。典型的身体活动计划包括 3 个 阶段:(1)准备活动:5~10 min轻度热身活动;(2)训 练阶段:20~30 min 有氧或耐力身体活动;(3)放松 阶段:约 5 min,逐渐减少用力,使心脑血管系统反 应和身体产热功能逐渐稳定。
5. 限制饮酒:限制饮酒与血压下降显著相关,并具有明显的量效关系,对于酒精摄入量大(每日 酒精摄入量>24 g)的高血压患者,减少酒精摄入可 显著降低血压[222]。酒精摄入量平均减少 67%,收 缩压下降 3.31 mmHg,舒张压下降 2.04 mmHg [223]。目前有关少量饮酒有利于心血管健康的证据不足, 相关研究表明即使少量饮酒的人减少酒精摄入也 可改善心血管健康,降低心血管病风险[224]。但对 于血压正常高值且有饮酒习惯的人群,减少饮酒量 并不能降低其高血压发病率[225]。
建议高血压患者不饮酒。如饮酒,每日酒精摄 入量男性不超过25 g,女性不超过15 g。
二、降压药物治疗
(一)概述
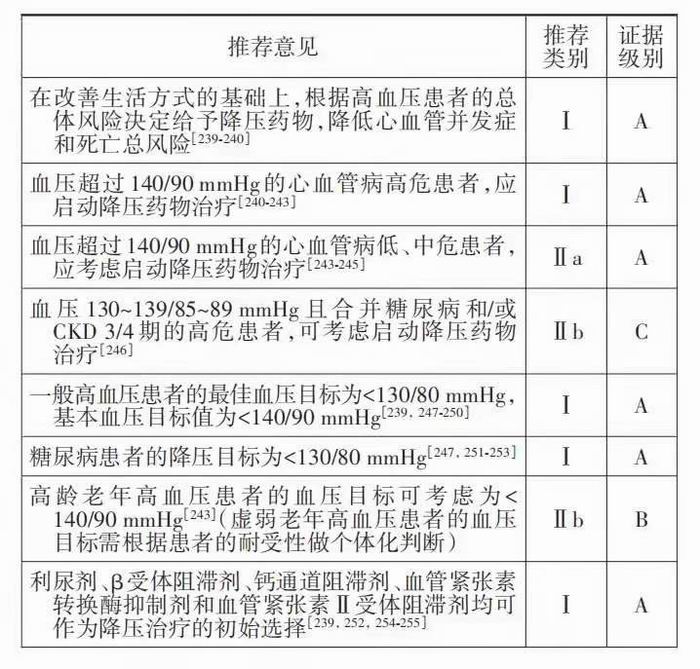
虽然积极改善生活方式可有效降低血压,但大部分高血压患者需要在改善生活方式的基础上接受降压药物治疗。既往有关降压治疗的临床试验为确定血压目标值和降压药物的选择提供了重要的依据。
(二)支持证据
1.降压药物治疗可显著降低心血管病风险:降 压药物治疗可显著降低高血压患者心、脑、肾并发 症和死亡总风险。收缩压降低 10 mmHg 或舒张压 降低 5 mmHg 可使主要心血管事件发生率降低 20%、总死亡率降低 10%~15%、卒中发生率降低 35%、冠心病发生率降低 20%、心力衰竭发生率降 低40%[239‐240]。无论基线血压和/或心血管病风险水 平如何,是否合并糖尿病和CKD,不同年龄、种族和 性别的高血压患者进行降压治疗均可降低相关事件的发生率[239,241],但正常高值人群降压治疗获益 仅限于合并冠心病者。
2. 强化降压治疗的疗效和安全性:ACCORD、 SPRINT 和 SPS3 研究[247‐249] 均是近期有关强化降压 (将收缩压降至 130 mmHg 以下)的研究,入选人群 分别为糖尿病、心血管病高危和腔隙性脑梗死患 者。入选人群按照血压目标分组,积极干预组的血 压分别降至 119、121 和 127 mmHg,虽然 ACCORD 研究中心血管主要终点事件发生情况组间差异未 见统计学意义,但强化降压组卒中发生率显著降低 (40%)。SPRINT研究中主要终点事件发生率组间 差异则有统计学意义(HR=0.75,95%CI 0.64~0.89, P<0.001)。SPS3 研究中主要终点事件(卒中)发生 率 有 降 低 趋 势(HR=0.81,95%CI 0.64~1.03,P= 0.08)。虽然 SPRINT 研究采用的无人看管的自动 血压测量方法与常规血压测量有所不同,可能影响 研究结果,但后续的荟萃分析结果仍支持强化降压 治疗[250]。
另一项荟萃分析显示,基线收缩压>160 mmHg 的患者,收缩压每降低 10 mmHg 主要心血管事件 和死亡的获益与基线血压 130~139 mmHg 的人群 类似,研究还显示收缩压<130 mmHg人群心血管事 件和死亡减少[239]。该分析结果显示强化降低收缩 压除可使有心血管合并症、糖尿病和 CKD 患者获 益外,无合并症患者也可获益,但此类患者多合并 多重心血管病危险因素。
ACCORD 和 SPRINT 研究结果显示,虽然强化 降压可增加不良反应,但并未增加严重不良反应。但 荟 萃 分 析 结 果 显 示 将 收 缩 压 进 一 步 降 至 120 mmHg以下,则因不良反应停药发生率增加[256]。
3. 1 级高血压患者的降压治疗:对 1 级高血压 (140~159/90~99 mmHg)患者进行药物治疗可降低 其心血管并发症的发生率[240‐242]。有关主要终点的 研究,即使是1级高血压无其他合并症的患者也因 存在多重危险因素或糖尿病,其心血管病风险多为 高危及以上,因此相关研究的证据主要局限于心血 管病高危患者。关于 1 级低中危高血压人群初始 降压药物治疗的直接证据主要来自HOPE3研究的 亚组分析,即中等风险的1级高血压患者(收缩压> 143.5 mmHg,平 均 154.1 mmHg),收 缩 压 降 低 6.0 mmHg时主要终点事件显著减少[243]。
4. 血压正常高值者的降压治疗:有研究入选了 无心血管并发症或糖尿病的血压为正常高值的人 群,发现使用血管紧张素Ⅱ受体阻滞剂和血管紧张素转换酶抑制剂治疗 2 年可降低此类人群高血压 的发病率[257‐258]。但心血管病低中危人群使用降压 药物未见心血管终点事件获益[246]。虽然目前仍缺 乏关于无心血管合并症的高危正常高值血压人群 降压药物治疗的研究,但因血压为 130~139/85~ 89 mmHg 且合并糖尿病或 CKD 3/4 期患者的血压 控制目标通常更为严格,使用降压药物是合理的。
5. 总体风险不同的患者降压治疗的效果存在 差异:根据总体风险对高血压患者进行降压治疗可 降低其总心血管并发症的发生率,总体风险不同疗 效不同[244‐245],基线风险越高治疗绝对获益越大,但 仍存在高剩余风险。对于心血管终点事件的影响, 无论基线总体风险如何,降压治疗获益主要来自减 少卒中事件。对于心血管病低危患者,降压治疗减 少心肌梗死、心力衰竭、心血管死亡和总死亡的疗效 有限。对于血压140/90 mmHg以下的患者,仅有证据 显示合并冠心病的高危患者可从降压治疗中获益[241]。
6.糖尿病患者降压治疗的获益:研究显示对于 合并高血压的 1 型糖尿病患者采用降压药物治疗 可改善其视网膜病变[259],尚缺乏有关心血管终点 事件的研究。
有关合并高血压的2型糖尿病患者的大规模临 床试验显示,降压治疗可显著减少其心血管并发症 和总死亡[251]。ACCORD研究强化降压治疗,即将收 缩压降至119 mmHg及以下,患者总心血管事件发生 率有降低趋势,其中卒中发生率降低显著[247]。荟 萃 分 析 同 样 显 示 2 型 糖 尿 病 患 者 血 压 降 至 130/80 mmHg以下,只有卒中发生率显著降低[252‐253]。对ACCORD研究进一步分析,排除降糖治疗的交互 作用后,发现收缩压降至130 mmHg以下患者总体心 血管事件发生率降低,但收缩压120 mmHg以下的患 者 心 血 管 事 件 有 增 加 趋 势[260]。支 持 舒 张 压 < 80 mmHg的证据主要来自ADVANCE和ACCORD研 究,强化血压控制组的舒张压均降至80 mmHg以下。
7.不同年龄人群血压的降压治疗:对 40~69岁 人群的队列随访研究发现,血压从115/75 mmHg开 始,舒张压每升高 10 mmHg,致死性卒中风险增加 2 倍,缺血性心血管病死亡风险增加 2 倍,在 80~ 89岁人群中血压水平与心血管病死亡仍存在正相关关系。随年龄增加,年病死率增加。不同性别间 年龄特异性相关的死亡男性和女性近似。
需注意,迄今为止有关老年高血压患者降压治 疗的研究均不包括虚弱老年人。这些试验,包括关 于 80 岁以上的老年高血压患者的临床试验,入选者的收缩压>160 mmHg,另外一些研究入选的老年 高血压患者在基线时已服用降压药物,为1级高血 压患者[243]。研究发现收缩压降至 140 mmHg 以下 可降低此类患者心血管事件发生率。虚弱老年人 的血压管理应避免降压过度致不耐受。
8.不同年龄、不同总体风险的高血压患者降压 治疗的费用效益:高风险人群治疗费效比最佳,而 对低心血管病风险人群需综合考虑患者意愿和费 用支出[261]。SPRINT 研究显示严格血压控制组治 疗费效比优于标准治疗组[262]。
9.不同降压药的疗效:降压治疗的获益主要来自 血压降低本身,五大类降压药物(利尿剂、β受体阻滞 剂、钙通道阻滞剂、血管紧张素转换酶抑制剂和血管 紧张素Ⅱ受体阻滞剂)在减少总心血管事件方面作 用近似[239,252,254‐255],均可作为降压治疗的初始选择。不同药物对于单一终点事件的影响不同,β受体阻滞 剂减少卒中的作用弱于其他四类降压药物,而钙通 道阻滞剂预防心力衰竭的作用较弱。不同药物有不 同的优势作用人群,对于不同靶器官损害人群的影 响不同。在不良反应方面也存在差异。单片固定复 方制剂有协同降压的作用,可改善患者依从性。其他 降压药物包括α受体阻滞剂、醛固酮受体拮抗剂、肾素抑制剂、中枢神经系统抑制剂,通常不作为首选药物。
血脂管理
一、血脂目标推荐
(一)概述
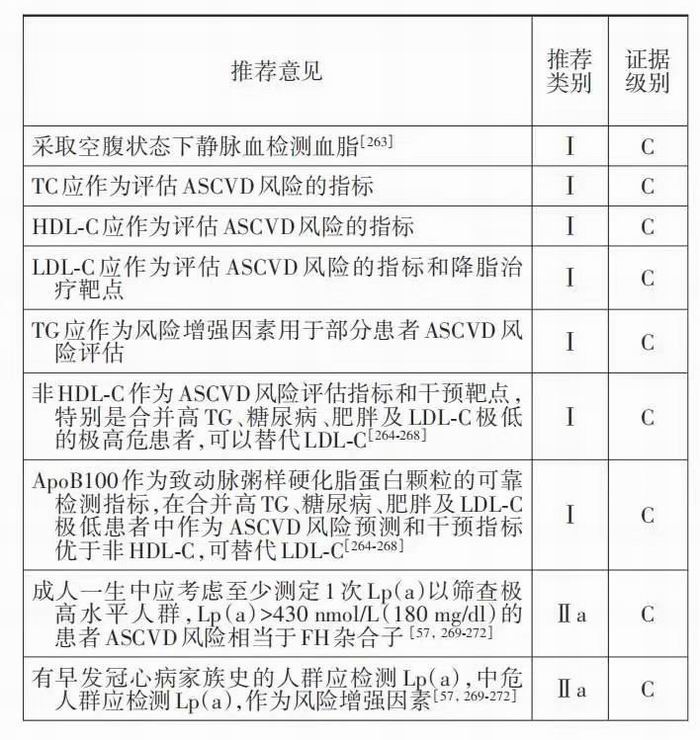
要评估个体的 ASCVD 风险,必须首先测定 血脂水平。Framingham 风险评估模型和汇总队 列方程中需测定 TC 和 HDL‐C[9]。在欧洲相关指 南的 ASCVD 风险评估模型(SCORE)中,TC 是重 要的评估指标,而 HDL‐C 可进一步增加风险评估的准确性[33]。LDL‐C 在所有的临床干预研究 中均作为治疗靶点和疗效判断指标,在中国的 ASCVD 风险评估模型中其也是重要的风险评估 因素[3]。ACC/AHA 以及 ESC 相关指南中的风险 评 估 模 型 ,只 纳 入 了 TC 和 HDL‐C 两 项 血 脂 指 标,这些模型主要源于早期(20 世纪 70 至 80 年 代)队列,当时主要关注这两个指标。但随着对血脂代谢异常认识的加深,发现其他血脂指标 对 ASCVD 风险也有独立预测价值。通常情况下 LDL‐C、非 HDL‐C 和 ApoB 相关性很好,但在部分 TG 升 高 的 患 者(如 肥 胖 、代 谢 综 合 征 及 糖 尿 病),LDL‐C 则不能准确反映 ASCVD 风险,因富 含 TG 的脂蛋白颗粒也是致动脉粥样硬化 ApoB 颗粒的重要组成成分,TG 升高时 LDL‐C 颗粒占 ApoB 颗粒的比重减少,此时单独检测 LDL‐C 容 易低估 ASCVD 风险。
Lp(a)是在低密度脂蛋白(LDL)颗粒表面结 合了载脂蛋白 a(Apo a)的脂蛋白,其与 LDL‐C 颗 粒一样能致动脉粥样硬化,而 Apo a 与纤溶酶原具 有类似结构,可与纤溶酶原受体结合,促进血栓形 成 。一 生 中 需 至 少 测 定 1 次 Lp(a)水 平 ,如 ≥ 430 nmol/L(180 mg/dl),则终生 ASCVD 风险显著 升高,相当于 FH 杂合子的风险。但在以往的 ASCVD 风险评估模型中没有纳入 Lp(a),2019 年 AHA 及 ESC 相关指南中均将其作为 ASCVD 风险 评估的辅助因素[9,33]。
(二)支持证据
血脂检测通常采集空腹(禁食 8 h 以上)静脉 血,餐后血标本的 TG 通常升高。虽然关于欧洲人 群的研究提示餐后LDL‐C水平变化不大,建议可采 用非空腹血脂[273],但国内研究显示普通饮食后 2~ 4 h LDL‐C水平有较大降幅(0.24~0.56 mmol/L)[263,274], 根据餐后LDL‐C水平可能高估降脂治疗的达标率, 因此仍建议采用空腹静脉血检测血脂作为 LDL‐C 达标的依据。
关于降脂目标的推荐目前存在争议,多数指 南推荐 LDL‐C 作为首要目标,非 HDL‐C 和 ApoB 作 为 次 要 目 标 ,但 有 研 究 显 示 非 HDL‐C 和/或ApoB 对 ASCVD 的预测价值优于 LDL‐C[264‐268]。因 此也有指南将非 HDL‐C 作为首要目标[275‐278]。本 《指南》推荐 LDL‐C 作为首要指标,非 HDL‐C 作为 替代指标。但对于合并糖尿病、代谢综合征、肥 胖及高 TG 患者,非 HDL‐C 作为首要目标。有关 Lp(a)的 观 察 性 研 究 显 示 参 考 Lp(a)可 增 加 ASCVD 危险分层的准确性[57,269‐272],虽不作为降脂 治疗的目标,但建议 ASCVD 中危以上的患者检测 Lp(a)。
二、降胆固醇目标推荐
(一)概述
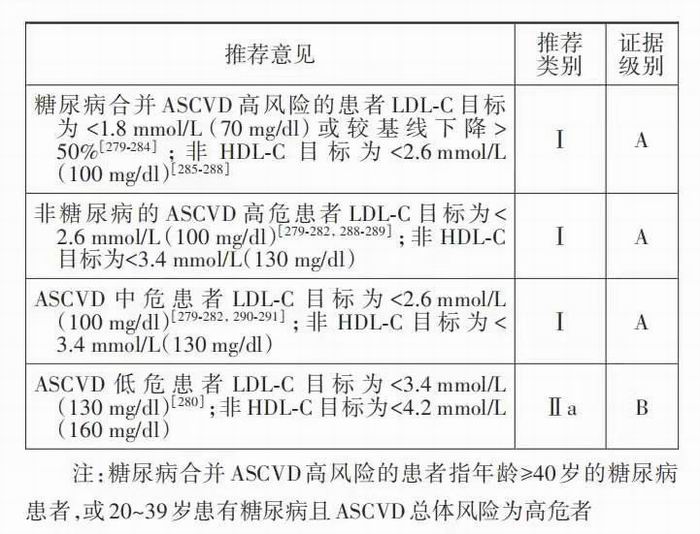
研究证实无论采用什么方式,将LDL‐C降得越低、持续时间越长,ASCVD 风险降低越多,目前未发现 LDL‐C 与 ASCVD 失关联的阈值。因此,理论上所有个体只要降低LDL‐C均可降低ASCVD发生风险。但考虑到药物治疗的成本及潜在的不良反应,目前临床上需根据 ASCVD 基线风险制定降脂目标。
(二)支持证据
有关ASCVD预防血脂目标设定的依据主要源于 RCT,部分来自于观察性研究和基因孟德尔RCT,尽管这些研究没有系统探索LDL‐C的特定目标值,但荟萃分析结果显示 LDL‐C 降低越多、持续时间越长,ASCVD 风险降低越多[279‐282]。研究未发 现LDL‐C降低的无效阈值,也未发现LDL‐C降低本 身的不良反应。LDL‐C 下降与 ASCVD 相对风险下 降呈线性相关,提示 LDL‐C 降得越低 ASCVD 风险 越低。但在确定LDL‐C治疗目标时,要考虑降脂的 成本效益。要保证合适的成本效益需考虑两项因 素,一是治疗后 LDL‐C 的绝对下降值,二是治疗对 象的基线风险。因此要根据基线ASCVD风险制定LDL‐C目标,即基线风险越高LDL‐C目标越低。虽然所有 ASCVD 高危患者的 LDL‐C 目标应一致,但考虑到糖尿病合并ASCVD高危患者的心血管事件风险更大其 LDL‐C 目标应更低。75岁以上的老年人群一级预防的降脂治疗证据不充分,因此没有特别推荐。同时,部分患者特别是基线 TG 升高的患者(如肥胖、代谢综合征及糖尿病患者),其 LDL‐C不能很好地代表所有致动脉粥样硬化脂蛋白,即含ApoB的脂蛋白,此时非HDL‐C可作为含ApoB脂蛋白的替代指标用于ASCVD风险评估。
虽然所有他汀类药物及近来的非他汀类药物的相关研究都以 LDL‐C 为目标,但有证据显示非 HDL‐C 能更好地代表致动脉粥样硬化脂蛋白颗粒[265‐266]。他汀类药物治疗的荟萃分析显 示,与 LDL‐C 比较非 HDL‐C 达标能更好地预测 ASCVD 剩余风险[267‐268],因此部分指南和共识将 非 HDL‐C 作 为 首 要 目 标[275‐278]。目 前 推 荐 的 非 HDL‐C 目 标 为 LDL‐C 目 标 +0.8 mmol/L[0.8 mmol 代表极低密度脂蛋白(VLDL)颗粒携带的胆固 醇],但非 HDL‐C 与 LDL‐C 差值受基线 LDL‐C 及 TG 水平影响,LDL‐C 与非 HDL‐C 的对比研究发 现,当 LDL‐C 为 2.6 mmol/L 时对应的非 HDL‐C 为 3.2 mmol/L,差值为 0.6 mmol/L[285‐286],与我国相关 研究结果一致[287]。所以当 LDL‐C 水平很低时 (<2.6 mmol/L),相 应 非 HDL‐C 目 标 的 增 加 值 (VLDL‐C)应 同 步 下 调( <0.8 mmol/L)。如 2017 年美国内分泌协会糖尿病管理指南首次将 ASCVD超高危患者LDL‐C目标值设为1.4 mmol/L, 而相应的非 HDL‐C 目标为 2.1 mmol/L[278]。鉴于 我 国 临 床 医 师 更 习 惯 以 LDL‐C 为 目 标 ,本《指 南》仍然推荐 LDL‐C 作为第一目标,非 HDL‐C 作 为替代目标。对 TG 升高人群(糖尿病、代谢综 合 征 、肥 胖 等)和 LDL‐C 较 低 但 ASCVD 极 高 危 的 人 群 应 采 用 非 HDL‐C 作 为 第 一 目 标 。非 HDL‐C 目标仍采用 LDL‐C 目标+0.8 mmol/L。
三、调脂治疗中的饮食管理
(一)概述
降低致动脉粥样硬化脂蛋白最基本的措施是 改善生活方式,其中饮食对血脂水平影响最大,健 康饮食是降低胆固醇的关键。
关于 ASCVD 一级预防中的饮食推荐,较为一 致的认识是推荐限制饱和脂肪酸及反式脂肪的 摄入[292‐294],增加果蔬、谷薯类及鱼类摄入的地中 海饮食模式[86]。对饮食胆固醇及鸡蛋的推荐存 在分歧。2015 至 2020 年美国饮食指南关于饮食 胆固醇推荐的描述存在矛盾,AHA/ACC 相关指南 提到胆固醇不应成为令人担忧的营养素[302],但 在 健 康 饮 食 模 式 中 却 提 到 应 尽 量 少 吃 胆 固 醇[303]。实际上胆固醇、饱和脂肪酸及动物蛋白 往往同时存在于食物中,很难界定胆固醇含量高 而饱和脂肪酸含量低的食物。关于饮食胆固醇 及鸡蛋摄入与血清胆固醇水平及 ASCVD 风险的 研究结果不一致。不同指南采纳不同研究结果 导致结论不同。
与欧美心血管病逐年下降的趋势不同,我国心 血管病发生呈上升趋势,且血脂异常人群也同步上 升,2012 至 2014 年人群血 LDL‐C 水平较 2002 年上 升了近 50%[21]。我国面临的严峻形势提示需加强 控制高胆固醇饮食的摄入,不能跟随欧美的饮食指 南放开对胆固醇的限制。建议针对不同人群设定 不同饮食胆固醇和鸡蛋黄的摄入标准,ASCVD 中 低危人群限制每日胆固醇摄入量<300 mg;对于高 危或血胆固醇水平升高的人群,每日胆固醇摄入量 应更低(<200 mg)。
(二)支持证据
1. 饮食中胆固醇含量影响血胆固醇水平:多数研究发现饮食胆固醇与血浆 LDL‐C 升高有 关。研究显示健康年轻男性每日消耗 0、1、2 和 4 个鸡蛋使胆固醇摄入量从 128 mg 逐渐增加至 858 mg 时,其血浆 LDL‐C 水平同步增加,饮食胆 固 醇 每 增 加 100 mg LDL‐C 增 加 1.5 mg/dl (0.04 mmol/L)[296]。而对于女性,饮食胆固醇对 血 浆 胆 固 醇 的 影 响 则 更 为 明 显 ,每 日 消 耗 0、 1 和 3 个鸡蛋使胆固醇摄入量从 108 mg 逐渐增 加至 667 mg 时,每增加 100 mg 饮食胆固醇血浆 LDL‐C 水 平 增 加 2.1 mg/dl(0.05 mmol/L)[295]。荟 萃 分 析 结 果 显 示 每 日 食 用 1~3 个 蛋 黄 可 使 LDL‐C 增 加 4~12 mg/dl(0.10~0.31 mmol/L),如 此 以往会产生很大不利影响。在饮食胆固醇摄入 与 血 胆 固 醇 关 系 中 ,胆 固 醇 摄 入 量 与 血 清LDL‐C 的关系较 HDL‐C 密切,因此研究者建议 限制鸡蛋摄入[304]。另一项荟萃分析结果显示 胆固醇摄入量减少 200 mg 可使血胆固醇降低约 4 mg/dl(0.1 mmol/L)[305]。2020 年 AHA 发布了饮 食胆固醇与心血管病的科学建议,认为饮食高 胆固醇与血胆固醇水平升高有关,但考虑到推 荐具体饮食胆固醇含量不易执行,遂只笼统推 荐 了 健 康 饮 食 模 式 ,如 地 中 海 饮 食 和 DASH 饮食[124]。
2. 鸡蛋及饮食中胆固醇影响 ASCVD 风险:一项前瞻性研究纳入了 5 672 例女性糖尿病患 者 ,发 现 每 摄 入 200 mg 胆 固 醇 或 1 000 kcal 热 量心血管病风险增加 37%[297]。另外一项研究 结 果 提 示 摄 入 鸡 蛋 增 加 新 发 糖 尿 病 风 险[306]。关 于 饮 食 对 临 床 终 点 的 影 响 很 难 进 行 RCT 设 计,多数为观察性研究,其结果受诸多混杂因 素影响,遂易出现矛盾。胆固醇基线水平可能 会影响饮食选择,如基线胆固醇水平高的人可 能较少吃鸡蛋或高胆固醇食物,而基线胆固醇 低的人则不然。荟萃分析也一样,当纳入的研 究 异 质 性 高 且 分 析 时 未 全 面 严 格 控 制 其 他 混 杂 因 素 时 ,很 难 得 出 一 致 结 论[122]。2019 年 一 项荟萃分析纳入了 6 项高质量队列研究,通过 去除极端饮食人群,统一量化每项研究的胆固 醇含量,采用不同模型控制了其他饮食成分的 影响,特别是控制了个体的总热量和基线胆固 醇水平,结果显示饮食中胆固醇含量及鸡蛋数 量与心血管病发生及全因死亡呈量效关系,每 日每增加 300 mg 胆固醇摄入,冠心病风险增加 17%、全因死亡增加 18%[299]。而其他发现胆固 醇 或 鸡 蛋 摄 入 不 影 响 心 血 管 病 风 险 的 荟 萃 分 析 均 未 对 基 线 胆 固 醇 水 平 及 总 热 量 进 行 控制[307‐309]。
3. 孟 德 尔 基 因 RCT 提 示 饮 食 胆 固 醇 影 响 ASCVD 风险:孟德尔基因 RCT 显示,与肠道胆固 醇吸收相关基因 NPC1L1 突变可导致 LDL‐C 水平 下降,NPC1L1 基因突变携带者 LDL‐C 水平平均下 降 12%,冠心病风险下降 53%[300]。另一项孟德尔 基因 RCT也显示,当 NPC1L1基因突变与胆固醇合 成相关的 HMGCR 基因突变导致 LDL‐C 同幅下降 时,其冠心病风险下降幅度相同[301]。提示抑制肠 道来源的胆固醇吸收与抑制肝脏胆固醇合成同样 能 减 少 ASCVD 风 险 ,间 接 支 持 应 限 制 胆 固 醇 摄入。
四、降胆固醇药物治疗
(一)概述
ASCVD 一级预防首先推荐健康生活方式,包括饮食、身体活动、控制体重、戒烟和限制饮酒等。当改善生活方式不能使血脂达标时应考虑药物治疗。降胆固醇药物在 ASCVD 预防中具有重要作用,根据机制可分为抑制胆固醇合成的他汀类药物、抑制胆固醇吸收的依折麦布及胆酸螯合剂以及抑制 LDL 受体降解的 PCSK9 抑制剂。上述三类药物是目前临床常用的降胆固醇药物。此外还有用于纯合子 FH 的特殊药物,包括抑制肝脏分泌VLDL的微粒体TG 转移蛋白(MTP)抑制剂(如洛美他派)和抑制VLDL载脂蛋白生成的Apo B100 反义核苷酸(如米泊美生)。纯合子FH是一类罕见血脂异常疾病,治疗较为特殊,已有专病指南,本《指南》不做讨论,但杂合子FH表型较为常见,其治疗措施与普通高危人群相同。
他汀类药物用于ASCVD一级预防证据最为充分。大量研究证实他汀类药物可显著降低高、中甚至低危人群的 ASCVD 风险。研究人群基线平均LDL‐C 水 平 从 192 mg/dl(4.9 mmo//L)到 108 mg/dl(2.8 mmol/L),包括高、中、低危人群,结果一致显示他汀类药物可显著降低 ASCVD 风险,且 LDL‐C 降低越多其风险降低越多。
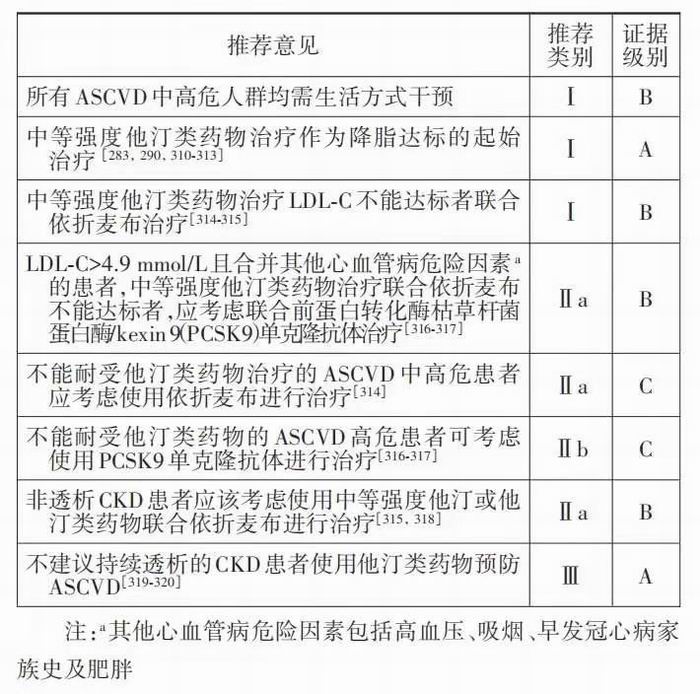
尽管他汀类药物是降胆固醇治疗的基础,但其剂量增加 1 倍 LDL‐C 降低效果只能增加 6%,且有潜在的不良反应,如肝功能损害、肌病及新发糖尿病等。结合我国人群对大剂量他汀的耐受性较欧美人群差,我们不建议使用高强度大剂量他汀,推荐起始使用中等剂量或中等强度他汀。不能耐受他汀或单独使用 LDL‐C 不能达标者可单独或联合使用非他汀类药物,如依折麦布、PCSK9 单克隆抗体。血脂康具有较好的安全性,在中国人群二级预防研究中显示出临床获益[321],可作为中等强度的 降胆固醇药物使用或他汀不耐受者的替代药物。
由于非他汀类药物的良好疗效及耐受性,中等强度他汀联合非他汀类药物达到强化降胆固醇目标已成为最常用的治疗方法。高危患者要达到LDL‐C下降50%,只有大剂量的强效他汀如阿托伐他汀 80 mg 或瑞舒伐他汀 20 mg 才能达到,但我国患者很少能耐受这种高强度的他汀长期应用。而多数中等强度他汀联合依折麦布 10 mg 或单独使 用PCSK9单克隆抗体均可达到上述目标[322]。鉴于 PCSK9单克隆抗体的价格较高,我们推荐降胆固醇 药物的顺序首先是中等强度他汀,不达标者联合应 用依折麦布;对于LDL‐C>4.9 mmol/L且合并其他心 血管病危险因素的高危患者,可考虑使用他汀联合 PCSK9单克隆抗体(表5)。
(二)支持证据
1. 他汀类药物与 ASCVD 一级预防:他汀类药 物在 ASCVD 一级预防中发挥作用的证据众多。WOSCOPS 研 究 纳 入 平 均 LDL‐C 为 192 mg/dl (4.9 mmol/L)但无明确心血管病者为研究对象,发 现普伐他汀 40 mg 可使一级终点事件发生率降低 31%、心血管死亡率降低 32%、全因死亡率降低 22%[310]。该研究人群的平均 LDL‐C 为 192 mg/dl (4.95 mmol/L),5 年非致死性心肌梗死及冠心病死 亡高达 7.9%,属于心血管病高危人群。在普通人 群 中 ,基 线 LDL‐C>190 mg/dl(4.9 mmol/L)者 较 LDL‐C<130 mg/dl(3.4 mmol/L)者 30 年 ASCVD 风险 高出 5 倍[43],提示 LDL‐C>190 mg/dl(4.9 mmol/L)时 需要积极进行降胆固醇治疗。HOPE3 研究针对 LDL‐C 不高、心血管病中危人群,入选时人群平均 LDL‐C 为 127.8 mg/dl(3.3 mmol/L),发现瑞舒伐他 汀 10 mg 可 使 其 心 血 管 病 风 险 降 低 24%[290]。JUPITER研究结果显示,即使是基线血脂水平偏低 [LDL‐C 108 mg/dl(2.8 mmol/L)]的低危人群,瑞舒 伐他汀 20 mg 也可使其心血管联合终点事件发生 率降低46%。JUPITER研究事后分析显示,根据对 瑞舒伐他汀反应的差异将治疗组人群分为 LDL‐C 降低≥50%和<50%组,与安慰剂组比较一级终点事件发生率分别低了 57% 和 39%[323],提示 LDL‐C 下 降>50%可作为强化降胆固醇获益的目标。首个有 关亚洲人群降胆固醇治疗与心血管病一级预防的 研究结果显示,与单纯饮食控制组比较,饮食控制+ 普伐他汀 10~20 mg组患者首次冠心病事件发生率 低了 33%[311]。关于糖尿病和高血压患者的一级预 防研究也证实心血管病高危人群可从中等强度他 汀类药物治疗中获益[283,312‐313]。
荟萃分析结果显示,无论是否存在基础心血管 病、基线心血管病风险如何[280]、基线 LDL‐C水平高 低[288]、他汀类药物种类和剂量如何,LDL‐C 每降低 1 mmol/L、持续 5 年,人群心血管病风险降低 21%、全因死亡风险下降12%[289]。
有关 75岁以上老年人他汀类药物心血管病一 级预防的证据较少。PROSPER 研究的对象为 70~ 82 岁老年人群,其中 50% 是心血管病高危人群, 50% 患有心血管病。结果显示,普伐他汀 40 mg组 主要不良心血管事件(MACE)风险较安慰剂低 15%[324]。2019年一项包括28项他汀类药物治疗相 关研究的荟萃分析显示,75 岁以上组及 75 岁及以 下 4 个年龄组人群均可能从他汀类药物治疗中获 益 ,但 没 有 基 础 心 血 管 病 的 两 个 老 年 组(70~ 75岁,>75岁)的获益程度有下降趋势[325]。
CKD 是 ASCVD 的高危因素,而他汀类药物降 低ASCVD风险的作用又受肾功能的影响。他汀类 药物可显著降低轻中度肾功能不全患者心血管病 的风险[326],但对于重度肾功能不全的患者其心血 管保护作用降低[319‐320]。荟萃分析结果显示他汀类 药物降低心血管病风险的幅度随 eGFR 下降而 下降[318]。
2. 非 他 汀 类 药 物 与 ASCVD 一 级 预 防 :EWTOPIA75 研究结果显示,依折麦布 10 mg 可使 75 岁及以上的无冠心病老年人群心脏性猝死、心 肌 梗 死 和 冠 状 动 脉 血 运 重 建 后 卒 中 风 险 下 降 34%[314]。提示依折麦布可作为老年人群ASCVD一 级预防用药。
有关他汀联合非他汀类药物心血管病一级预 防的研究较少。SHARP研究是以CKD患者为对象 的联合降脂心血管病保护作用的研究。该研究纳 入了无明确心血管病史的中重度 CKD 患者(包括 透析和非透析者),采用辛伐他汀 20 mg 联合依折 麦布 10 mg进行干预,尽管与安慰剂组比较联合治 疗组患者平均LDL‐C仅低了0.85 mmol/L,但其非致 死性心肌梗死、心原性死亡、非出血性卒中及血运 重建风险低 17%。提示辛伐他汀 20 mg 联合依折 麦 布 10 mg 可 降 低 中 重 度 CKD 患 者 ASCVD 风险[315]。
目前尚缺乏单纯PCSK9抑制剂在ASCVD一级 预防中作用的研究。2 项短期探索性研究纳入了 ASCVD 高危人群及患者,发现在他汀类药物治疗 的基础上加用 PCSK9 抑制剂可显著减少心血管事 件风险。OSLER 研究的对象为 4 465 例结束了依 洛尤单抗 2~3期研究的患者,按 2∶1比例随机分为 常规他汀治疗+依洛尤单抗组和常规他汀治疗组。平均随访11.1个月,结果显示依洛尤单抗组患者平 均LDL‐C水平由120 mg/dl(3.1 mmol/L)降至48 mg/dl(1.2 mmol/L)(降幅61%),1年心血管事件风险下降 53%。该研究人群80%具有心血管病危险因素,但 只有20%存在基础冠心病[316]。因此该研究可视为 ASCVD高危人群一级预防的证据。ODDYSSEY 长 期研究纳入ASCVD高危患者2 341例(其中70%患 有冠心病),按2∶1比例随机分为常规他汀治疗+阿 立西尤单抗组和常规他汀治疗组,随访78周,结果 显示与常规他汀治疗组比较,阿立西尤单抗组 LDL‐C 水平低了 62%,心血管不良事件风险低了 48%。该研究中只有 30% 的人符合 ASCVD 一级预 防标准[317]。
五、TG管理与ASCVD一级预防
(一)概述
富含 TG 的 VLDL 颗粒及残粒携带了循环中的 大部分TG。TG升高与ASCVD风险增加相关,但校 正非 HDL‐C 后二者的相关性消失[55]。同样,如果 按非 HDL‐C 变化幅度计算,贝特类药物降低 TG 对 ASCVD 风险的影响与相同降幅的 LDL‐C 一致[281], 提示降低 TG 对 ASCVD 的影响是通过降低涵盖了 富含 TG 脂蛋白的非 HDL‐C 来实现的。此外,孟德 尔基因 RCT 也支持 TG 与冠心病具有因果关系,但 需注意这些基因对 HDL‐C、LDL‐C 或 Lp(a)亦有影 响。2019年的一项基因 RCT发现,当降 TG相关脂 蛋白酯酶(LPL)基因变异与降 LDL‐C 相关 LDL 受 体基因变异导致 ApoB 变化幅度相同时,他们对 ASCVD 风险的影响也相同[331]。提示富含 TG 脂蛋 白及其残粒与 ASCVD 的因果关系是由 ApoB 脂蛋 白颗粒而不是TG本身决定的。既往研究发现即使 在校正LDL-C的作用后,贝特、烟酸及n-3脂肪酸3种 降TG药物使用后TG降低仍与MACE减少相关。
TG 升高与不良生活方式及饮食密切相关,身 体活动和饮食控制可减少肥胖及胰岛素抵抗,从而 有效降低TG,饮酒是TG升高的非常重要的危险因 素,对于TG高的人群酒精摄入量限制应更为严格。饮食中除限制脂肪酸摄入外,还需注意减少精制碳 水化合物摄入,应多摄入富含纤维素的低糖食物 (如全谷类粗粮)。
(二)支持证据
1. 贝 特 类 药 物 与 ASCVD 一 级 预 防 :CPIT、 HHS、 VA‐HIT、 BIP、 LEADER、 FIELD[329] 和 ACCORD[332] 研究是目前我们检索到的有关贝特类 药物与临床终点事件的 RCT 研究,共 7 项。FIELD 研究的对象为2型糖尿病患者,其中78%入选时无 心血管病病史或证据,发现进行了一级预防的人群 其主要和次要终点事件发生率分别下降 25% 和 11%[329],证明非诺贝特可减少 ASCVD 高危人群的 心血管事件。ACCORD 研究是首个他汀类药物联 合贝特类药物的大规模 RCT。研究对象为 2 型糖尿病患者,其中 74% 既往无心血管病史,入选者在 辛伐他汀治疗基础上随机进行非诺贝特或安慰剂 治疗。结果显示两组间主要和次要终点事件发生 率差异均无统计学意义。进一步对 TG≥204 mg/dl (2.3 mmol/L)伴HDL‐C≤34 mg/dl(0.88 mmol/L)的亚 组人群进行分析,发现非诺贝特可使复合终点事件 的发生率减少 31%[332],提示他汀类药物联合贝特 类药物可减少高 TG、低 HDL‐C 的糖尿病患者的心血管事件。荟萃分析结果显示,贝特类药物减少高 TG、低HDL‐C人群的心血管事件[333‐335]。总体而言, 目前贝特类药物可减少心血管事件的证据远不如 他汀类药物充分。
2. n‐3脂肪酸对心血管病的影响:几项大规模的 RCT(如ORIGIN、ASCEND、VITAL研究)均显示,低 剂量n‐3脂肪酸(1 g/d)并不能降低ASCVD高危患者 的心血管病风险[336‐338]。n‐3脂肪酸的作用可能与剂 量及种类有关。如JELIS研究纳入18 645例胆固醇 升 高 的 患 者 ,在 他 汀 治 疗 的 基 础 上 随 机 分 为 1.8 g EPA干预组和安慰剂组,结果显示EPA干预组 MACE 发生率降低 19%(P=0.011)[327]。REDUCE‐IT 研究的对象为他汀类药物治疗后 TG 仍高(1.7~ 5.6 mmol/L)的患者,给予 IPE 4 g/d 或安慰剂(矿物 油)进行干预,结果显示与安慰剂组比较IPE 4 g/d组 的患者主要心血管病终点事件发生率低 25%(P< 0.001)[328],需要注意的是该研究中 70.7% 为二级预 防 的 人 群 ,一 级 预 防 的 人 群 仅 占 29.3%。STRENGTH研究纳入了接受他汀类药物治疗后TG 仍高的ASCVD高危人群,随机给予高剂量n‐3脂肪 酸(EPA+DHA 4 g/d)或安慰剂(玉米油)治疗[339],随 访5年左右时因两组心血管事件发生率差异无统计 学意义而终止研究。提示n‐3脂肪酸对于ASCVD的 预防作用不仅与剂量有关,还可能与种类有关。
2型糖尿病管理
(一)概述
2 型糖尿病是 ASCVD 的主要危险因素[35]。对 2 型糖尿病患者进行针对 ASCVD 危险因素的长期 强化综合治疗可显著降低其心血管事件风险[351‐352]。
此外,关于糖耐量异常人群,“大庆糖尿病预防 研究”及长期随访发现,适度控制碳水化合物及酒 精摄入、增加蔬菜摄入以及合理进行身体活动等生 活方式综合干预,有助于延缓糖耐量异常人群发展 至临床糖尿病的进程,并减少其心血管事件和死亡。
(二)支持证据
1. 有益于心血管健康的饮食模式是 2 型糖尿 病治疗的重要手段:地中海饮食与DASH饮食及素 食均被证明有助于减重、改善2型糖尿病患者的血 糖控制[340‐341,353]。同时,研究已证实遵循健康饮食 模式的 2 型糖尿病患者发生心血管病及相关死亡 的风险显著降低[351]。
碳水化合物的种类对控制 2 型糖尿病尤其重 要,应摄入膳食纤维丰富的全谷物(粗粮、杂粮),避 免摄入精米精面等精制碳水化合物[354]。一项基于 美国糖尿病患者的前瞻性队列研究显示,摄入不饱 和脂肪酸较多与总死亡率和心血管病死亡率较低 相关,提示摄入脂肪的种类对2型糖尿病患者心血 管病预防也有重要作用[355]。我国队列研究显示摄 入红肉与2型糖尿病风险增加相关[356];美国队列研 究则证明减少红肉摄入可改善血糖控制[357];瑞典 一项前瞻性队列研究显示 2 型糖尿病患者食用鱼肉与心肌梗死发生率降低有关[358];日本一项基于 亚洲糖尿病患者的队列研究显示,2型糖尿病患者 肉类摄入量增加与心血管病发病率升高相关[359]。减重是2型糖尿病患者的基本治疗手段,超重和肥 胖者应减重[212,360‐362]。营养计划的制定应在专业人 员的指导下完成。
2. 身体活动有助于 2 型糖尿病患者的血糖及 心血管病危险因素控制:一项关于RCT的荟萃分析 显示身体活动可降低糖尿病患者的糖化血红蛋白 水平[363]。与单一类型的身体活动比较,有氧联合 阻力训练改善血糖控制、促进减重的效果更为显 著[342‐343]。运动训练可改善 2 型糖尿病患者的心脏 自主神经功能[364]。一项前瞻性队列研究发现,包 含中高强度身体活动在内的健康生活方式与低心 血管病发生率及死亡率相关[365]。此外,有 RCT 表 明长期中等强度连续训练联合阻力训练以及高强 度间歇训练联合阻力训练均可降低 2 型糖尿病患 者IMT。此外,高强度间歇训练可改善外周动脉僵 硬度指数及扩张系数[366]。
对于老年尤其是有其他合并症的 2 型糖尿病 患者,可以采用步行等简单的身体活动方式。相对 健康的年轻患者,鼓励采用多种身体活动方式。除 了规律进行身体活动的方案外,还应鼓励增加日常 身体活动(如爬楼梯、步行或骑行等)。
3. 二甲双胍治疗与心血管病风险降低相关:UKPDS 研究对新诊断并伴有超重的 2 型糖尿病患 者随机分组,发现与其他传统疗法(如仅改善生活 方式)比较,二甲双胍可使糖尿病相关的微血管和 大血管并发症的发生率降低32%,心肌梗死的发生 率降低 39%,全因死亡率降低 36%[344]。2016 年一 项关于 2 型糖尿病降糖治疗的系统综述和荟萃分 析支持二甲双胍作为治疗2型糖尿病的一线药物, 其对降低糖化血红蛋白水平、控制体重和改善 ASCVD结局有益,且安全性较好、成本低廉[345]。二 甲双胍有导致乳酸酸中毒的风险,故 eGFR<30 ml· min-1·1.73m-2的 4期 CKD患者禁用。对于多数 2型 糖尿病患者,若无禁忌证,建议在生活方式干预的 同时启动二甲双胍治疗;对于年轻或仅有糖化血红 蛋白轻微升高的患者,可先进行3~6个月的生活方 式干预,然后根据血糖及时启动二甲双胍治疗。
4.SGLT‐2 抑制剂可减少 ASCVD 高危的成年 2型糖尿病患者的心血管事件:SGLT‐2抑制剂作用 于肾近端小管,抑制其对葡萄糖的重吸收,促进葡 萄糖从尿液中排泄,从而降低血糖水平。研究表明使用 SGLT‐2 抑制剂恩格列净、卡格列净及达格列 净均可显著降低 2 型糖尿病患者复合心血管事件 发生率和心力衰竭住院率[348‐349,367‐371]。虽然大多数 受试者在基线时已患有心血管病,但其降低心力衰 竭住院率的作用已被证明可扩大至一级预防人 群[349,372‐375]。此外,有关卡格列净及达格列净的临 床试验 CANVAS 和 DECLARE,分别纳入了 34.4% 和 59.4% 的存在高危因素但尚未发生 ASCVD 的 2型糖尿病患者,结果显示SGLT‐2抑制剂可降低此 类患者肾功能衰竭和心力衰竭住院的风险,可考虑 将其用于心血管病一级预防[348‐349]。
5.GLP‐1 受体激动剂可减少 ASCVD 高危的成 年 2 型糖尿病患者的心血管事件:GLP‐1 受体激动 剂以葡萄糖依赖的方式增强胰岛素分泌、抑制胰高 血糖素分泌,并能延缓胃排空,通过中枢性的食欲 抑制减少进食量。部分GLP‐1受体激动剂(如利拉 鲁肽、阿必鲁肽、司美格鲁肽、度拉糖肽)可降低成 年 2 型糖尿病患者的 ASCVD 风险[350,376‐378]。关于 GLP‐1 受 体 激 动 剂 的 临 床 试 验 ,LEADER、 SUSTAIN‐6 和 REWIND 分别纳入了 27.6%、27.8% 和 68.5% 存在高危因素但尚未发生 ASCVD 的 2 型 糖尿病患者,其中仅REWIND研究提供了GLP‐1受 体激动剂用于 2 型糖尿病患者心血管病一级预防 的证据[350,376‐380]。
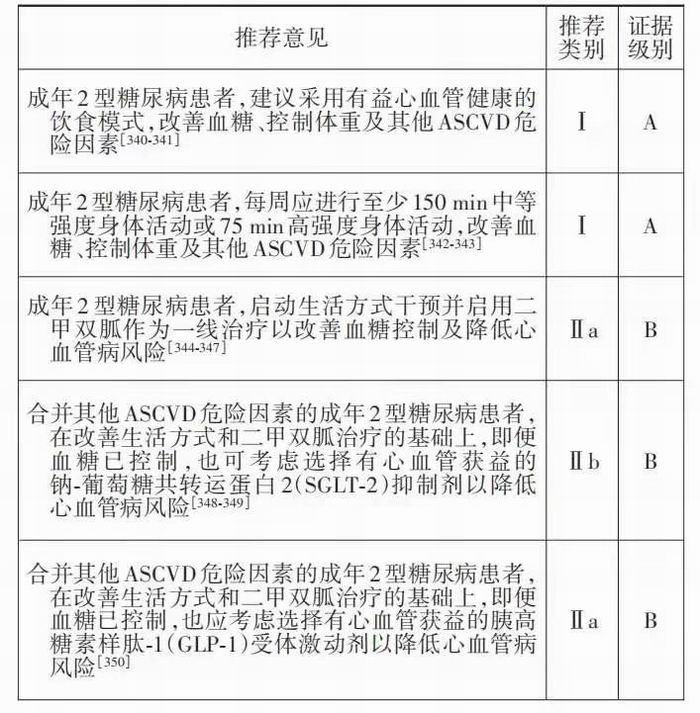
基于当前证据,对于合并心血管病危险因素的 2 型糖尿病患者在生活方式干预和二甲双胍治疗 的基础上,无论血糖是否控制,在可及和可负担的 情况下启用有心血管获益证据的SGLT‐2抑制剂或 GLP‐1 受体激动剂进行心血管病一级预防是合理的。
阿司匹林的使用
(一)概述
阿司匹林的主要作用机制是通过不可逆地抑 制环氧合酶 1的活性和血栓烷 A2依赖性血小板凝 集,降低血栓形成风险,但其可增加出血风险,尤其 是胃肠道出血[391]。阿司匹林曾广泛用于 ASCVD 一级和二级预防,现有证据提示 ACSVD 的一级预 防应基于临床获益和风险比,进行个体化治疗。
(二)支持证据
1. 阿司匹林的获益:阿司匹林在 ASCVD 二级 预防的应用被广泛认可[8,392],但其在一级预防中的 应用争议较大。我国目前尚缺乏评估阿司匹林在 ASCVD一级预防中疗效和安全性的前瞻性大规模 临床研究。国内外最新指南对于阿司匹林一级预 防推荐的意见也不一致,欧洲指南不建议其用于 ASCVD 一级预防[8]。基于 2016年以前公布的研究 的荟萃分析显示,阿司匹林的主要获益为降低心肌 梗死事件的趋势尤其是非致死性心肌梗死、降低缺 血性卒中,全因死亡率有降低趋势。但同时,严重 出血和胃肠道出血均明显增加。我国和美国相关 指南曾建议将阿司匹林用于 ASCVD 高风险患 者[393‐394]。而2016年以后公布的研究结果显示阿司 匹林的获益有减少的趋势[395‐397],尤其是在减少非 致命性心肌梗死及缺血性卒中方面。相较于血压 控制和降胆固醇治疗,阿司匹林用于 ASCVD 一级 预防的获益较小而出血风险较高[381‐388],国外新近 发 表 的 相 关 研 究(ASCEND、ARRIVE、ASPREE 等)[395‐398]使阿司匹林的推荐级别进一步降低。在 临床中需平衡患者的缺血和出血风险,合理使用阿 司匹林。
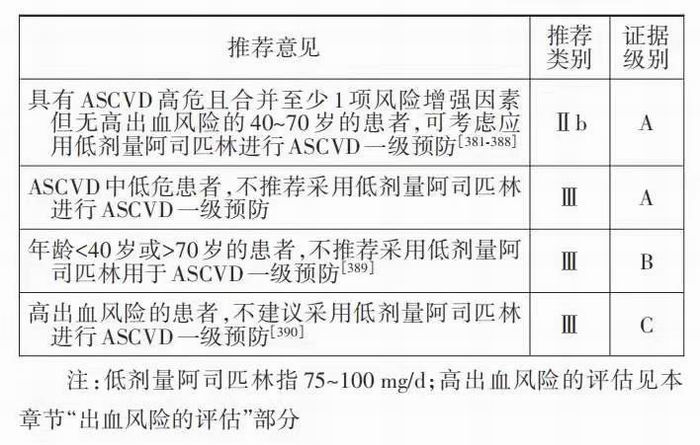
2. 缺血风险的评估:ASCVD 防治中抗血小板 治疗的重要性在于减少急性血栓形成事件,如何识 别高缺血风险患者是适应证选择的重要依据。ASCVD高风险患者预防性应用阿司匹林的获益风 险比更佳[393,399],以往研究中观察到的事件发生率 与预估的 ASCVD 风险相关性较好。因此,对于 10 年 ASCVD 风险≥10% 的患者服用阿司匹林的获 益风险比较好[394,400]。但近期的临床研究观察到的 实际事件风险低于预估的 ASCVD 风险[396]。因此, 应识别缺血危险程度更高的一级预防人群,建议在 高危人群基础上综合考虑传统危险因素以外的增 强因素,如早发心肌梗死家族史,血脂、血压或血糖 控制不佳,CAC积分明显较高等(详见“心血管病风 险评估”部分)[401]。尽管2016年以后的研究中阿司 匹林的获益风险比减少,但仍有部分患者预防性使用阿司匹林带来的心血管获益大于风险。对于存 在增强因素、无法调控其他因素的 ASCVD 高风险 患者,预防性应用低剂量阿司匹林可作为治疗策略 之 一[402]。ASCVD 低 危 患 者 不 建 议 使 用 阿 司 匹林[396]。
3.出血风险的评估:考虑使用阿司匹林时应进 行出血风险评估。阿司匹林可增加严重出血风险, 尤 其 是 胃 肠 道 出 血 ,但 不 增 加 致 命 性 出 血 风 险[387,390,397]。与安慰剂比较,阿司匹林不增加颅内 出血风险,硬膜外和硬膜下出血的风险每 1 000 人 年增加1例,亚组分析显示颅内出血风险的高危人 群为亚裔和低体重者[403]。出血高危险因素包括但 不限于以下情况:既往有胃肠道出血或消化性溃疡 疾病,既往有重要脏器出血史,低体重、年龄> 70岁、血小板减少、凝血功能障碍、CKD、同时使用 增加出血风险的药物(如非甾体类抗炎药、类固醇、 非维生素 K 拮抗剂口服抗凝药和华法林等)[390]。适用阿司匹林进行一级预防的患者,可使用质子泵 抑制剂预防消化道出血[404‐405]。
4.阿司匹林的推荐剂量:因阿司匹林一级预防 利弊之间的总体差异较小,一般推荐阿司匹林剂 量≤100 mg/d。荟萃分析证据提示小剂量应用阿司 匹林的 ASCVD 风险获益等同于大剂量阿司匹林, 但大剂量应用阿司匹林的出血风险较高[392]。不同 体重的人使用标准剂量的阿司匹林风险获益比不 同[406],但尚需前瞻性研究进一步证实。目前建议 阿司匹林一级预防的剂量为75~100 mg/d。
5. 阿司匹林的适用年龄:使用阿司匹林进行 ASCVD一级预防时,对于年龄>70岁的患者其风险 大于获益,不建议常规使用[389]。对于年龄<40岁的 患者,目前尚缺乏足够证据判断常规应用阿司匹林 的 风 险 获 益 比 。尽 管 如 此 ,仍 可 根 据 已 知 的 ASCVD风险增强因素和出血风险,对于年龄<40岁 或>70岁的患者进行个体化评估和讨论,以决定是 否需要预防性使用小剂量阿司匹林。
主要执笔人:
刘静(首都医科大学附属北京安贞医院),孙艺红 (中日友好医院),彭道泉(中南大学湘雅二医院),张宇清(中国医学科学院 阜外医院),刘靖(北京大学人民医院)
核心专家:高润霖(中国医学科学院 阜外医院),赵冬(首都医科大学附属北京安贞医院),王继光(上海交通大学医学院附属瑞金医院 上海市高血压研究所),叶平(解放军总医院第二医学中心),郭艺芳(河北省人民医院),杨新春(首都医科大学附属北京朝阳医院),陈鲁原(广东省人民医院),李建军(中国医学科学院 阜外医院),程翔(华中科技大学同济医学院附属协和医院)
专家委员会成员(按姓氏拼音排序):
边惠萍(青海省心脑血管病专科医院),蔡军(中国医学科学院 阜外医院),陈桂英(哈尔滨医科大学附属第一医院),陈红(北京大学人民医院),陈纪言(广东省人民医院),陈晓平(中日友好医院),陈桢玥(上海交通大学医学院附属瑞金医院),陈鲁原(广东省人民医院),程翔(华中科技大学同济医学院附属协和医院),戴若竹(福建医科大学附属泉州第一医院),丁荣晶(北京大学人民医院),丁世芳(中部战区总医院),董吁钢(中山大学附属第一医院),范志清(大庆油田总医院),冯颖青(广东省人民医院),傅向华(河北医科大学第二医院),高润霖(中国医学科学院 阜外医院),郭建军(首都体育学院),郭艺芳(河北省人民医院),韩雅玲(北部战区总医院),候静波 (哈尔滨医科大学附属第二医院),胡大一(北京大学人民医院),黄恺(华中科技大学同济医学院协和医院 华中科技大学同济医学院梨园心血管临床中心),纪立农(北京大学人民医院),贾绍斌(宁夏医科大学总医院),江洪(武汉大学人民医院),荆志成(中国医学科学院 北京协和医院),黎励文(广东省人民医院),李春坚(江苏省人民医院),李建军(中国医学科学院 阜外医院),李凌(郑州大学第一附属医院),李晓东(中国医科大学附属盛京医院),李新立(南京医科大学第一附属医院),李毅(北部战区总医院),李玉明(泰达国际心血管病医院),梁春(上海长征医院),刘靖(北京大学人民医院),刘静(首都医科大学附属北京安贞医院),刘培良(辽宁省金秋医院),马长生(首都医科大学附属北京安贞医院),孟晓萍(长春中医药大学附属医院),宁光(上海交通大学医学院附属瑞金医院),宁毅(北京大学医学部美年公众健康研究院),彭道泉(中南大学湘雅二医院),齐晓勇(河北省人民医院),曲鹏(大连医科大学附属第二医院),沈玉芹(同济大学附属同济医院),史旭波(首都医科大学附属北京同仁医院),孙艺红(中日友好医院),唐熠达(北京大学第三医院),王东伟(郑州市中心医院),王继光(上海交通大学医学院附属瑞金医院 上海市高血压研究所),王乐民(同济大学附属同济医院),王守力(战略支援部队特色医学中心),王效增(北部战区总医院),吴永健(中国医学科学院 阜外医院),肖丹(国家呼吸医学中心 中日友好医院烟草病学与戒烟中心),肖新华(中国医学科学院 北京协和医院),徐标(南京大学医学院附属鼓楼医院),许俊堂(北京大学人民医院),闫承慧(北部战区总医院),杨丽霞(解放军联勤保障部队第九二〇医院),杨新春(首都医科大学附属北京朝阳医院),叶平(解放军总医院第二医学中心),于淼(中国医学科学院 北京协和医院),余金明(复旦大学公共卫生学院),袁晋青(中国医学科学院 阜外医院),袁祖贻(西安交通大学第一附属医院),张存泰(华中科技大学同济医学院附属同济医院),张剑(北部战区总医院),张俊杰(南京市第一医院),张瑞岩(上海交通大学医学院附属瑞金医院),张啸飞(清华大学北京清华长庚医院),张瑶俊(徐州市第三人民医院),张宇清(中国医学科学院 阜外医院),赵冬(首都医科大学附属北京安贞医院),赵文华(中国疾病预防控制中心营养与健康所),周胜华(中南大学湘雅二医院),周迎生(首都医科大学附属北京安贞医院),周玉杰(首都医科大学附属北京安贞医院)
利益冲突 所有作者均声明不存在利益冲突
参考文献略
来源:中华心血管病杂志